题目内容
NA为阿伏加德罗常数,下列叙述正确的是( )
| A、12 g金刚石中含有的共价键数为2NA |
| B、22.4LNH3中含有的电子数为10NA |
| C、将1molCl2通入足量水中充分反应达到平衡后转移电子总数为NA |
| D、电解精炼铜时,当电路中转移2NA个电子时粗铜的质量减少64g |
考点:阿伏加德罗常数
专题:
分析:A、金刚石中,每个C与其它4个C形成了四个共价键,根据均摊法计算出1molC含有的共价键;
B、氨气所处的状态不明确;
C、Cl2与水的反应是可逆反应;
D、电解精炼阳极失电子的不全是铜.
B、氨气所处的状态不明确;
C、Cl2与水的反应是可逆反应;
D、电解精炼阳极失电子的不全是铜.
解答:
解:A、12g金刚石中含有1molC,金刚石中,每个C与其它4个C形成了4个共价键,每个碳原子形成的共价键数目为:
×4=2,所以1molC原子形成的共价键为2mol,含有的共价键数目为2NA,故A正确;
B、氨气所处的状态不明确,故22.4L氨气的物质的量不一定是1mol,故B错误;
C、Cl2与水的反应是可逆反应,不能进行彻底,故转移电子总数小于NA,故C错误;
D、电解精炼阳极失电子的不全是铜,还有锌、镍、铁等金属,依据电子守恒可知,阳极铜质量减少的质量不是64g,故D错误;
故选A.
| 1 |
| 2 |
B、氨气所处的状态不明确,故22.4L氨气的物质的量不一定是1mol,故B错误;
C、Cl2与水的反应是可逆反应,不能进行彻底,故转移电子总数小于NA,故C错误;
D、电解精炼阳极失电子的不全是铜,还有锌、镍、铁等金属,依据电子守恒可知,阳极铜质量减少的质量不是64g,故D错误;
故选A.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构、状态是解题关键,难度不大.

练习册系列答案
相关题目
反应SiCl4+2H2
Si(纯)+4HCl可用于工业制取纯硅.该反应属于( )
| ||
| A、化合反应 | B、复分解反应 |
| C、置换反应 | D、分解反应 |
下列有关二氧化硫的说法中,错误的是( )
| A、二氧化硫的水溶液能使紫色石蕊试液变红,说明它能和水反应生成H2SO3 |
| B、二氧化硫能漂白某些物质,说明它具有氧化性 |
| C、将足量二氧化硫通入酸性高锰酸钾试液中,溶液褪色,说明二氧化硫具有还原性 |
| D、实验室可用浓硫酸干燥二氧化硫气体 |
下列叙述不正确的是( )
| A、虽然石墨有较好的导电性,但它不属于电解质 |
| B、CaCO3、BaSO4都难溶于水,但它们都是电解质 |
| C、实验测定液态HCl、固体KNO3均不能导电,所以HCl、KNO3均是非电解质 |
| D、酒精(纯净物)在水溶液和熔融状态下均不能导电,所以酒精属于非电解质 |
在同温同压下,10L气体A2跟30L气体B2恰好完全化合生成20L气体C,则气体C的化学式(用A、B表示)为( )
| A、AB |
| B、A2B |
| C、AB2 |
| D、AB3 |
下列化学用语表示不正确的是( )
| A、氮化镁的化学式:MgN | ||||
B、中子数为18的氯原子:
| ||||
| C、Ca(OH)2的电离方程式:Ca(OH)2═Ca2++2OH- | ||||
D、铁在氯气中燃烧:2Fe+3Cl2
|
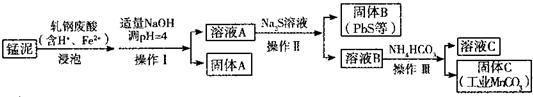
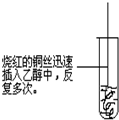 乙醇的催化氧化,看右图答出实验现象.
乙醇的催化氧化,看右图答出实验现象.