题目内容
下列实验不能达到目的是( )
| 实验 |  |  |  |  |
| 目的 | 测量锌与稀硫酸的反应速率 | 向容量瓶中转移溶液 | 鉴别胶体和溶液 | 排除碱式滴定管尖嘴部分的气泡 |
| 选项 | A | B | C | D |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.应用分液漏斗;
B.转移溶液需要引流;
C.丁达尔效应是胶体的特性;
D.气泡密度较小,将胶管弯曲使玻璃尖嘴斜向上,捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,可将气泡赶出.
B.转移溶液需要引流;
C.丁达尔效应是胶体的特性;
D.气泡密度较小,将胶管弯曲使玻璃尖嘴斜向上,捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,可将气泡赶出.
解答:
解:A.应用分液漏斗,无法测出气体的体积,故A错误;
B.转移溶液需要用玻璃棒引流,故B正确;
C.溶液无丁达尔效应,胶体有丁达尔效应,故C正确;
D.气泡密度较小,将胶管弯曲使玻璃尖嘴斜向上,捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,可将气泡赶出,故D正确.
故选A.
B.转移溶液需要用玻璃棒引流,故B正确;
C.溶液无丁达尔效应,胶体有丁达尔效应,故C正确;
D.气泡密度较小,将胶管弯曲使玻璃尖嘴斜向上,捏住胶管,轻轻挤压玻璃珠,使溶液从尖嘴流出,可将气泡赶出,故D正确.
故选A.
点评:本题考查较为综合,涉及化学反应速率测定、容量瓶的使用,胶体的性质、滴定管的使用等操作,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意把握实验方法和注意事项,难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
FeO/Fe3O4广泛用于热化学循环分解水制取氢气.已知:H2O(g)+3FeO
Fe3O4+H2 (g)…①2Fe3O4
6FeO+O2 (g)…②下列说法正确的是( )
| ||
| ||
| A、反应①、②均是置换反应 |
| B、反应①中FeO被还原 |
| C、反应②中铁元素的化合价升高 |
| D、反应②中Fe3O4既是氧化剂又是还原剂 |
关于浓硫酸的叙述正确的是( )
| A、浓硫酸具有吸水性,因而能使蔗糖炭化 |
| B、浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 |
| C、常温下,金属铁遇浓硫酸时会在表面生成致密的氧化膜而发生钝化 |
| D、50mL 18mol?L-1硫酸中加入足量的铜粉反应放出二氧化硫气体少于10.08L |
可用如图所示装置制取、干燥、收集并吸收多余气体的是( )
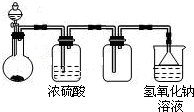

| A、浓氨水与氧化钙固体反应制氨气 |
| B、稀硫酸与硫化亚铁固体反应制硫化氢 |
| C、浓盐酸与次氯酸钙固体反应制氯气 |
| D、饱和食盐水与电石反应制乙炔 |

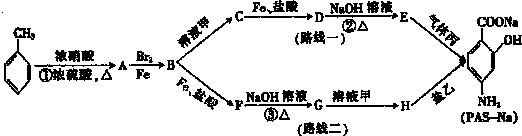
 (苯胺,易被氧化)
(苯胺,易被氧化)