题目内容
下列离子方程式正确的是( )
| A、钠投入到水中 2Na+2H2O═2Na++2OH-+H2↑ |
| B、铁与盐酸的反应 2Fe+6H+═2Fe3++3H2↑ |
| C、铁片插入氯化铁溶液中 Fe+Fe3+═2Fe2+ |
| D、氯化铝溶液中滴入过量氨水 Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、钠和水反应生成氢氧化钠和氢气;
B、铁与盐酸的反应生成氯化亚铁和氢气;
C、选项中离子方程式电荷不守恒;
D、氯化铝溶液中滴入过量氨水生成氢氧化铝沉淀和氯化铵.
B、铁与盐酸的反应生成氯化亚铁和氢气;
C、选项中离子方程式电荷不守恒;
D、氯化铝溶液中滴入过量氨水生成氢氧化铝沉淀和氯化铵.
解答:
解:A、钠和水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故A正确;
B、铁与盐酸的反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C、选项中离子方程式电荷不守恒,反应的离子方程式为:Fe+2Fe3+═3Fe2+,故C错误;
D、氯化铝溶液中滴入过量氨水生成氢氧化铝沉淀和氯化铵,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D正确;
故选AD.
B、铁与盐酸的反应生成氯化亚铁和氢气,反应的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C、选项中离子方程式电荷不守恒,反应的离子方程式为:Fe+2Fe3+═3Fe2+,故C错误;
D、氯化铝溶液中滴入过量氨水生成氢氧化铝沉淀和氯化铵,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+,故D正确;
故选AD.
点评:本题考查了离子方程式书写原则和正误判断,掌握书写方法和物质性质是解题关键,题目较简单.

练习册系列答案
相关题目
某无色透明的溶液能与Al作用放出H2,该溶液中可能大量共存的离子组是( )
| A、Na+、H+、NO3-、SO32- |
| B、H+、K+、CO32-、Cl- |
| C、NH4+、Cl-、Fe2+、OH- |
| D、Na+、K+、OH-、CO32- |
由甲酸甲酯、葡萄糖、乙醛、丙酸四种物质组成的混合物,已知其中氧元素的质量分数为37%,则氢元素的质量分数为( )
| A、54% | B、63% |
| C、9% | D、12% |
主链上有4个碳原子的某烷烃,有两种同分异构体,该烃的碳原子数是( )
| A、4个 | B、5个 | C、6个 | D、7个 |
被称为人体冷冻学之父的罗伯特?埃廷格(Robert Ettinger)在1962年写出《不朽的前景》(The Prospect Of Immortality)一书.他在书中列举了大量事实,证明了冷冻复活的可能.比如,许多昆虫和低等生物冬天都冻僵起来,春天又自动复活.下列结论中与上述信息相关的是( )
| A、温度越低,化学反应越慢 |
| B、低温下分子无法运动 |
| C、温度降低,化学反应停止 |
| D、化学反应前后质量守恒 |
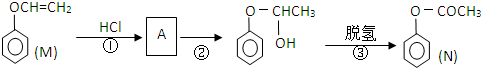
 )是一种重要的化工原料,请回答下列问题:
)是一种重要的化工原料,请回答下列问题: )的流程如下(条件略)
)的流程如下(条件略)