题目内容
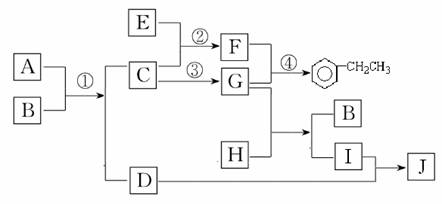
气体A的产量是衡量一个国家石油化工发展水平的标志,D是食醋中的主要成分.A能发生以下转化:
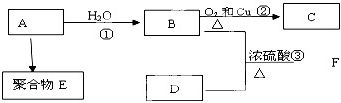
(1)A的结构简式为:
(2)E是(写结构简式)
 ;D中含氧官能团名称
;D中含氧官能团名称
(3)写出相应转化过程的反应化学方程式
②
③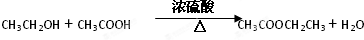
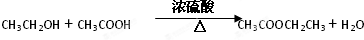 反应类型:
反应类型:

(1)A的结构简式为:
CH2=CH2
CH2=CH2
.(2)E是(写结构简式)


羧基
羧基
;(3)写出相应转化过程的反应化学方程式
②
2CH3CH2OH+O2
2CH3CHO+H2O
| Cu |
2CH3CH2OH+O2
2CH3CHO+H2O
反应类型:| Cu |
氧化
氧化
反应③
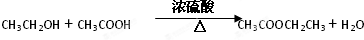
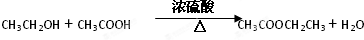
酯化(或取代反应)
酯化(或取代反应)
反应.分析:气体A的产量是衡量一个国家石油化工发展水平的标志,则A是乙烯,D是食醋中的主要成分则D是乙酸,乙烯和水发生加成反应生成乙醇,则B是乙醇,乙醇和乙酸发生酯化反应生成F,F是乙酸乙酯,乙醇在铜作催化剂、加热条件下发生氧化反应生成乙醛,则C是乙醛,乙烯发生加聚反应生成E,则E是聚乙烯.
解答:解:气体A的产量是衡量一个国家石油化工发展水平的标志,则A是乙烯,D是食醋中的主要成分则D是乙酸,乙烯和水发生加成反应生成乙醇,则B是乙醇,乙醇和乙酸发生酯化反应生成F,F是乙酸乙酯,乙醇在铜作催化剂、加热条件下发生氧化反应生成乙醛,则C是乙醛,乙烯发生加聚反应生成E,则E是聚乙烯,
(1)通过以上分析知,A是乙烯,其结构简式为:CH2=CH2,
故答案为:CH2=CH2;
(2)E是聚乙烯,其结构简式为: ,D的结构简式为:CH3COOH,其官能团名称是羧基,
,D的结构简式为:CH3COOH,其官能团名称是羧基,
故答案为: ,羧基;
,羧基;
(3)在铜或银作催化剂、加热条件下,乙醇被氧气氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
2CH3CHO+H2O,该反应属于氧化反应,
在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,反应方程式为: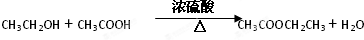 ,该反应属于酯化反应(或取代反应),
,该反应属于酯化反应(或取代反应),
故答案为:2CH3CH2OH+O2
2CH3CHO+H2O,氧化反应,
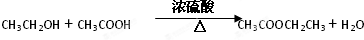 ,酯化反应(或取代反应).
,酯化反应(或取代反应).
(1)通过以上分析知,A是乙烯,其结构简式为:CH2=CH2,
故答案为:CH2=CH2;
(2)E是聚乙烯,其结构简式为:
 ,D的结构简式为:CH3COOH,其官能团名称是羧基,
,D的结构简式为:CH3COOH,其官能团名称是羧基,故答案为:
 ,羧基;
,羧基;(3)在铜或银作催化剂、加热条件下,乙醇被氧气氧化生成乙醛,反应方程式为:2CH3CH2OH+O2
| Cu |
在浓硫酸作催化剂、加热条件下,乙醇和乙酸发生酯化反应生成乙酸乙酯,反应方程式为:
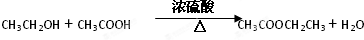 ,该反应属于酯化反应(或取代反应),
,该反应属于酯化反应(或取代反应),故答案为:2CH3CH2OH+O2
| Cu |
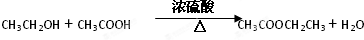 ,酯化反应(或取代反应).
,酯化反应(或取代反应).点评:本题考查了有机物的推断,明确常见有机物的反应、反应条件、官能团及其性质即可解答,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目