题目内容
8.下列说法正确的是( )| A. | 甲烷是最简单的烃,其含碳量最高 | |
| B. | 可以利用燃烧的现象鉴别甲烷和乙烯 | |
| C. | 乙醇、乙酸均能与钠反应放出H2,二者分子中官能团相同 | |
| D. | 乙烯、聚乙烯和苯分子均含有碳碳双键 |
分析 A.甲烷是最简单的烷烃,其含氢量最高;
B.乙烯含碳量高,火焰明亮;
C.乙醇、乙酸分别含有羟基、羧基;
D.聚乙烯、苯不含碳碳双键.
解答 解:A.甲烷是最简单的烷烃,其含氢量最高,含碳量最低,故A错误;
B.甲烷燃烧火焰呈淡蓝色,乙烯含碳量高,火焰明亮,由较浓的烟生成,现象不同,可鉴别,故B正确;
C.乙醇、乙酸分别含有羟基、羧基,二者都可与钠反应生成氢气,故C错误;
D.聚乙烯为乙烯的加聚产物,不含碳碳双键,苯结构特殊,碳碳键介于单键和双键之间,不含碳碳双键,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析、实验、评价能力的考查,注意把握物质的性质的异同以及实验的严密性、合理性的评价,难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
18.碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛.完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜.写出该反应的化学方程式4KI+2CuSO4=I2+Cu2I2↓+2K2SO4.
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去.写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是H2SO3、KI、Cu2I2.
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2+Hg═Cu2HgI4(玫瑰红)+2Cu,产物Cu2HgI4中Cu元素显+1价.当有1molCu2I2参与反应时,转移电子1mol.
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作.试剂M和操作N的组合正确的是bd(选填编号)
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜.写出该反应的化学方程式4KI+2CuSO4=I2+Cu2I2↓+2K2SO4.
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去.写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是H2SO3、KI、Cu2I2.
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:2Cu2I2+Hg═Cu2HgI4(玫瑰红)+2Cu,产物Cu2HgI4中Cu元素显+1价.当有1molCu2I2参与反应时,转移电子1mol.
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作.试剂M和操作N的组合正确的是bd(选填编号)
| 选项 | 试剂M | 操作N |
| a | 碘化钾溶液 | 升华 |
| b | 氢碘酸溶液 | 萃取分液 |
| c | 氢气 | 过滤 |
| d | 氢硫酸溶液 | 过滤 |
16.下列有关化学用语表示正确的是( )
| A. | 水分子的比例模型: | B. | F-的结构示意图: | ||
| C. | CO2的结构式:O-C-O | D. | 中子数为8的碳原子: |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1 mol Na与乙醇完全反应,失去2 NA个电子 | |
| B. | 常温常压下,8 g CH4含有5 NA个电子 | |
| C. | 1 L 0.1 mol•L-1的醋酸溶液中含有0.1 NA个H+ | |
| D. | 标准状况下,22.4 L苯含有NA个C6H6分子 |
17.可用于鉴别以下三种化合物的一组试剂是( )
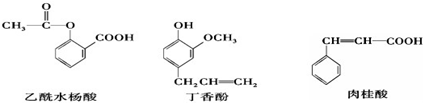
①溴的四氯化碳溶液 ②银氨溶液 ③三氯化铁溶液 ④氢氧化钠溶液.

①溴的四氯化碳溶液 ②银氨溶液 ③三氯化铁溶液 ④氢氧化钠溶液.
| A. | ②④ | B. | ①③ | C. | ③④ | D. | ①② |



 的路线如下:
的路线如下:
 和(CH3)2SO4为原料制备
和(CH3)2SO4为原料制备 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:CH3CHO$→_{催化剂,△}^{O_{2}}$CH3COOH$→_{浓H_{2}SO_{4},△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.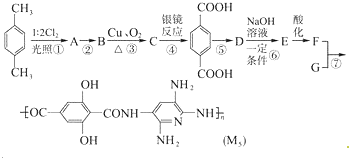
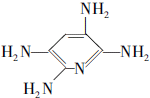 ,F的含氧官能团的名称有羧基、(酚)羟基.
,F的含氧官能团的名称有羧基、(酚)羟基.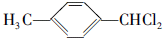 .
.