题目内容
常温下,下列各组离子在指定溶液中能大量共存的是( )
| A、在PH=0的无色溶液中:Na+、Fe3+、I-、SiO32- |
| B、滴入酚酞显红色的溶液中:Na+、S2-、SO32-、AlO2- |
| C、c(Fe2+)=1mo1?L-1的溶液中:H+、Na+、Cl-、NO3- |
| D、加入铝粉能产生大量H2的溶液中:Na+、NO3-、NH4+、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.PH=0的无色溶液,显酸性,并结合常见离子的颜色分析;
B.滴入酚酞显红色的溶液,显碱性;
C.离子之间发生氧化还原反应;
D.加入铝粉能产生大量H2的溶液,为非氧化性酸或强碱溶液.
B.滴入酚酞显红色的溶液,显碱性;
C.离子之间发生氧化还原反应;
D.加入铝粉能产生大量H2的溶液,为非氧化性酸或强碱溶液.
解答:
解:A.PH=0的无色溶液,显酸性,H+、SiO32-结合生成沉淀,Fe3+、I-发生氧化还原反应,不能共存,且Fe3+为黄色,故A错误;
B.滴入酚酞显红色的溶液,显碱性,该组离子之间不反应,能共存,故B正确;
C.Fe2+、H+、NO3-离子之间发生氧化还原反应,不能大量共存,故C错误;
D.加入铝粉能产生大量H2的溶液,为非氧化性酸或强碱溶液,HCO3-与酸、碱均反应,且碱性溶液中不能存在NH4+,酸溶液Al、H+、NO3-发生氧化还原反应不生成氢气,故D错误;
故选B.
B.滴入酚酞显红色的溶液,显碱性,该组离子之间不反应,能共存,故B正确;
C.Fe2+、H+、NO3-离子之间发生氧化还原反应,不能大量共存,故C错误;
D.加入铝粉能产生大量H2的溶液,为非氧化性酸或强碱溶液,HCO3-与酸、碱均反应,且碱性溶液中不能存在NH4+,酸溶液Al、H+、NO3-发生氧化还原反应不生成氢气,故D错误;
故选B.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应及氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
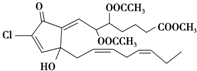 从一种珊瑚中分离出的活性含氯化合物punaglandin具有很强的抗癌活性,它的结构简式如图,有关该化合物的说法正确的是( )
从一种珊瑚中分离出的活性含氯化合物punaglandin具有很强的抗癌活性,它的结构简式如图,有关该化合物的说法正确的是( )| A、分子有3种含氧官能团 |
| B、分子中所有碳原子可以处于同一平面 |
| C、1mol该物质最多消耗4mol NaOH或3mol Br2 |
| D、该物质中只有一种官能团能使酸性高锰酸钾溶液褪色 |
苯甲酸的重结晶实验中,粗苯甲酸溶解后还要加点水的目的是( )
| A、无任何作用 |
| B、可以使过滤时速度加快 |
| C、减少过滤时苯甲酸的损失 |
| D、以上都不对 |
在下列溶液中,各组离子一定能够大量共存的是( )
| A、使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ |
| B、由水电离的c(H+)=1×10-14mol?L-1的溶液中:NH4+、K+、Cl-、CO32- |
| C、使酚酞变红的溶液中:Na+、C6H5O-、CH3COO-、CO32- |
| D、能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、I-、SO32- |
能用离子方程式“H++OH-═H2O”表示的化学反应是( )
| A、2NaOH+Si02═Na2Si03+H20 |
| B、HN03+KOH═KN03+H20 |
| C、S03+H20═H2S04 |
| D、2HCl+Na2C03═2NaCl+H20+C02↑ |
下列轨道上的电子在xy平面上出现的机会为零的是( )
| A、3Pz |
| B、3Px |
| C、3Py |
| D、3S |
2012年4月,中央电视台曝光了不法商贩将重金属铬(Cr)超标的工业明胶加工成药用胶囊的“毒胶囊”事件.已知铬的原子序数为24,一种同位素的质量数为53,下列叙述正确的是( )
| A、铬位于元素周期表的第Ⅷ族 | ||
| B、铬所在的周期有18种元素 | ||
| C、其原子质量是12C原子质量的53倍 | ||
D、中子数为29,铬原子符号表示为
|
对于化合物 ,下列叙述中正确的是( )
,下列叙述中正确的是( )
 ,下列叙述中正确的是( )
,下列叙述中正确的是( )| A、其化学式为C12H12 |
| B、分子中所有原子有可能处于同一平面 |
| C、该化合物分子中所有原子不可能处于同一平面 |
| D、分子中所有原子一定处于同一平面 |