题目内容
6.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),主要工艺流程如下.
(1)将过程②产生的气体通入下列溶液中,溶液会褪色的是ACD(填字母).
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程①中,FeS、O2和H2SO4反应的化学方程式为4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S.
(3)过程③中需加入的物质是Fe(或铁).
(4)过程④中,蒸发结晶时需使用的仪器除酒精灯、三脚架外,还需要蒸发皿、玻璃棒.
(5)过程⑤调节pH可选用下列试剂中的C(填字母).
A.稀硫酸 B.CaCO3 C.NaOH溶液.
分析 硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),烧渣在硫酸溶液中通入足量氧气,反应后过滤得到固体W和溶液X,溶液X加入铁反应生成硫酸亚铁,蒸发浓缩结晶析出得到绿矾,溶液X中加入试剂调节溶液PH得到溶液Z加热制备聚铁胶体得到聚铁,
(1)过程②产生的气体为SO2,具有还原性和漂白性;
(2)根据反应物和生成物的种类结合质量守恒书写化学方程式;
(3)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+;
(4)蒸发结晶需要使用酒精灯、三角架、蒸发皿、玻璃棒等仪器;
(5)过程⑤调节pH应使溶液碱性增强,有利于聚铁的生成.
解答 解:硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),烧渣在硫酸溶液中通入足量氧气,反应后过滤得到固体W和溶液X,溶液X加入铁反应生成硫酸亚铁,蒸发浓缩结晶析出得到绿矾,溶液X中加入试剂调节溶液PH得到溶液Z加热制备聚铁胶体得到聚铁,
(1)过程②产生的气体为SO2,具有还原性和漂白性,因具有漂白性而使品红褪色,因具有还原性而使具有氧化性的酸性KMnO4溶液、溴水褪色,故答案为:ACD;
(2)反应物为FeS、O2和H2SO4,生成物有S,根据质量守恒还应有Fe2(SO4)3和H2O,
反应的化学方程式为4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S,
故答案为:4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S;
(3)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+,加入铁可生成Fe2+,并且不引入新的杂质,
故答案为:Fe(或铁);
(4)蒸发结晶需要使用酒精灯、三角架、蒸发皿、玻璃棒等仪器,可能还需要泥三角,
故答案为:蒸发皿、玻璃棒;
(5)过程⑤调节pH应使溶液碱性增强,有利于聚铁的生成,
A.加入硫酸不能使溶液PH增大,故A错误;
B.加入碳酸钙生成微溶的硫酸钙,会引入新的杂质,故B错误;
C.加入NaOH可使溶液碱性增强,生成的聚铁中不引入新的杂质,故C正确.
故答案为:C.
点评 本题考查较为综合,涉及物质含量的测定、制备实验方案的设计等知识,题目难度中等,注意常见化学实验操作方法.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 钢铁在潮湿的空气中容易生锈 | |
| B. | 降低盐酸浓度以减缓盐酸与Zn反应的速率 | |
| C. | SO2氧化成SO3的反应,往往需要使用催化剂 | |
| D. | 恒温恒压的容器中有2NO2?N2O4,若通入Ar,气体的颜色先变浅后逐渐加深 |
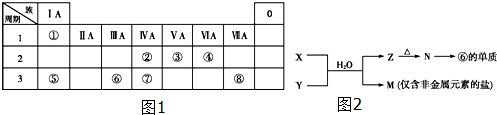
(1)写出由④、⑤、⑧元素形成的既含离子键又含共价键的一种离子化合物的化学式:NaClO.
(2)含元素⑧的单质能与自来水中的有机物反应生成对人体有危害的物质,现已逐步淘汰.下列可代替它作自来水消毒剂的是AC.
A.ClO2 B.AlCl3 C.K2FeO4
(3)W与④是相邻的同主族元素.在下表中写出H2WO3相应性质的化学方程式.
| 编号 | 性质 | 化学方程式 |
| 1 | 还原性 | H2SO3+Br2+2H2O═H2SO3+2HBr |
| 2 | 酸性 | H2SO3+2NaOH=Na2SO3+2H2O |
X溶液与Y溶液反应的离子方程式为Al3++3NH3+3H2O═Al(OH)3↓+3NH4+;
M中阳离子的鉴定方法是取少量M样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子;
如果M中含有元素⑧,M溶液中离子浓度由大到小的排列顺序是c(Cl-)>c(NH+4)>c(H+)>c(OH-).
| A. | 乙酸是一种弱酸,不能和碳酸钙反应放出二氧化碳气体 | |
| B. | 润滑油属于酯类 | |
| C. | 没有成熟的苹果汁遇碘变蓝色,成熟的苹果汁能还原新制氢氧化铜悬浊液 | |
| D. | 糖类、油脂、蛋白质都是由C、H、O三种元素组成 |
| A. | M的单质具有两性,所以能与NaOH溶液发生反应生成氢气 | |
| B. | Z、W、M的氧化物均可做耐高温材料 | |
| C. | 工业上常用电解熔融氯化物的方法制备Z、W的单质 | |
| D. | Y的单质都有剧毒,而且其着火点低,常保存在冷水中 |
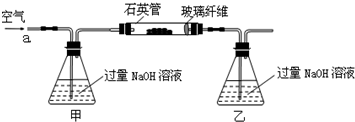
其反应的化学方程式为:
4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
4FeS+7O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4SO2
【实验一】:测定硫元素的含量反应结束后,将乙瓶中的溶液进行如下处理:

(1)鼓入空气的作用是提供反应需要的氧气,排出装置中生成的二氧化硫被乙装置全部吸收.
(2)反应结束后乙瓶中的溶液需加足量H2O2溶液的目的是Na2SO3+H2O2=Na2SO4+H2O(用化学方程式表示).
(3)该黄铁矿石中硫元素的质量分数为$\frac{32{m}_{2}}{233{m}_{1}}$×100%(列出表达式即可).
【实验二】:测定铁元素的含量
①用足量稀硫酸溶解石英管中的固体残渣→②加还原剂使溶液中的Fe3+恰好完全转化为Fe2+后,过滤、洗涤→③将滤液稀释至250mL→④取25.00mL稀释液用0.1 000mol/L的酸性KMnO4溶液滴定
(4)②中,若用铁粉作还原剂,则所测得的铁元素的含量偏大(填“偏大”、“偏小”或“无影响”).
(5)③中,需要用到的仪器除烧杯、玻璃棒、胶头滴管外,还有250mL容量瓶.
(6)某同学一共进行了四次滴定实验,实验结果记录如下:
| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 消耗KMnO4溶液体积/mL | 25.00 | 25.03 | 20.00 | 24.97 |
| A. | pH=7的溶液 | |
| B. | c(OH-)=$\sqrt{{K}_{W}}$ | |
| C. | 由强酸与强碱等物质的量反应得到的溶液 | |
| D. | 强电解质溶于水得到的溶液 |
 、
、 ,该反应的化学方程式为:2CO2+Na2O2═2Na2CO3+O2.
,该反应的化学方程式为:2CO2+Na2O2═2Na2CO3+O2.