题目内容
在10L密闭容器中,发生如下反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均反应速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为[ ]
4NO(g)+6H2O(g)。半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均反应速率υ(X)(反应物的消耗速率或产物的生成速率)可表示为[ ]
A.υ(NH3)=0.0100mol·L-1·s-1 B.υ(O2)=0.0010mol·L-1·S-1
C.υ(NO)=0.0010mol·L-1·s-1 D.υ(H2O)=0.045mol·L-1·s-1
【答案】
C
【解析】

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应的体系,当在某一温度时,A、B、C物质的量与时间的关系如图1,C的百分含量与温度的关系如图2.
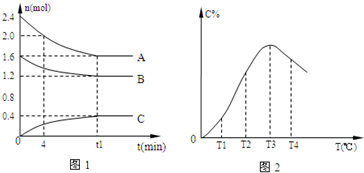
下列分析不正确的是( )

下列分析不正确的是( )
| A、0~4分钟时,A的平均反应速率为0.02mol/(L?min) | ||
B、该反应的平衡常数表达式K=
| ||
| C、由T1向T2变化时,V正>V逆 | ||
| D、此反应的正反应为放热反应 |


 在10L密闭容器中,某放热反应进行过程在不同反应时间各物质的量的变化情况如图所示(A、B、C均为气体),则:
在10L密闭容器中,某放热反应进行过程在不同反应时间各物质的量的变化情况如图所示(A、B、C均为气体),则: