题目内容
4. 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子,就像一尊释迦牟尼佛.有关该有机分子的说法正确的是( )| A. | 该有机物属于芳香烃 | B. | 该有机物属于苯的同系物 | ||
| C. | 该有机物分子中含有23个碳原子 | D. | 该有机物的一氯代物有3种 |
分析 A.含有苯环的烃是芳香烃;
B.苯的同系物含有1个苯环,侧链为烷基;
C.键线式中交点、端点为C原子,结合有机物结构的交点判断C原子数目;
D.根据等效氢进行判断.
解答 解:A.由结构简式可知,该物质只含C、H两种元素,分子中含有苯环,属于芳香烃,故A正确;
B.苯的同系物含有1个苯环,侧链为烷基,该烃不是苯的同系物,故B错误;
C.该有机物结构简式中交点为碳原子,分子中含有22个碳原子,故C错误;
D.该有机物分子为左右对称,分子中含有6种化学环境不同的H原子,其一氯代物有6种,故D错误.
故选A.
点评 本题考查有机物的结构与性质,为高考常见题型,把握习题中的信息及结构的对称性为解答的关键,注意苯的同系物的结构特点:含有1个苯环,侧链为烷基,题目难度中等.

练习册系列答案
相关题目
12.下列有关甲苯的实验事实中,能说明侧链对苯环性质有影响的是( )
| A. | 甲苯与硝酸发生取代反应生成三硝基甲苯 | |
| B. | 甲苯能使热的酸性高锰酸钾溶液褪色 | |
| C. | 甲苯燃烧时产生带浓烈黑烟的火焰 | |
| D. | 1mol甲苯最多能与3mol氢气发生加成反应 |
19.下列物质中,既有离子键又有共价键的是( )
| A. | MgCl2 | B. | Ca(OH)2 | C. | H2O | D. | C60 |
9.已知W、X、Y、Z为短周期元素,W、Z同主族,X、Y、Z同周期,W 的气态氢化物的稳定性大于Z的气态氢化物的稳定性,X、Y为金属元素,X的阳离子的氧化性小于Y的阳离子的氧化性.下列说法正确的是( )
| A. | 若W与Y的原子序数相差5,则二者形成化合物的化学式一定为Y2W3 | |
| B. | W与X形成的化合物中只含离子键 | |
| C. | W的气态氢化物的沸点一定高于Z的气态氢化物的沸点 | |
| D. | X、Y、Z、W的原子半径依次减小 |
16.已知①H2SO4比HClO4稳定 ②HClO4比H2SO4酸性强 ③S2-比Cl-易被氧化 ④HCl比H2S稳定 ⑤Cu与HCl不反应,与浓H2SO4反应,其中可以说明氯比硫非金属性强的是( )
| A. | 除①外 | B. | ②③④ | C. | ①②④ | D. | 全部 |
13.设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 20℃时,1mol SO2的体积一定大于22.4L | |
| B. | 常温常压下,1mol CO2与18 g H2O所含有的原子总数均为3 NA | |
| C. | 1mol/LNaCl溶液表示1L水中含有NaCl 58.5g | |
| D. | 标准状况下,11.2L NO与5.6 L O2形成的混合气体中含有的分子数为0.5NA |
14.金属元素铊的相关信息如图所示.下列有关卡片信息解读正确的是( )
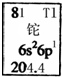

| A. | 铊元素的质量数是81 | B. | 铊原子的电子数为3 | ||
| C. | 铊原子的相对原子质量是204.4 | D. | 铊的金属性比铝的金属性强 |

