题目内容
将一小块银白色的金属钠放在空气中会发生一系列的变化:表面迅速变暗→“出汗”→变成白色固体粉末,下列有关叙述不正确的是( )
| A、表面迅速变暗是因为钠与空气中的氧气反应生成了氧化钠 |
| B、“出汗”是因为生成的氢氧化钠吸收空气中的水蒸气在表面形成了溶液 |
| C、最后变成的白色固体粉末是碳酸钠 |
| D、该过程的所有化学反应均为化合反应 |
考点:钠的化学性质,钠的重要化合物
专题:几种重要的金属及其化合物
分析:A.金属钠在空气中易氧化形成氧化钠,出现变暗现象;
B.氧化钠与空气中的水反应生成氢氧化钠,NaOH具有吸水性;
C.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水,最终变成白色粉末为碳酸钠;
D.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水是复分解反应;
B.氧化钠与空气中的水反应生成氢氧化钠,NaOH具有吸水性;
C.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水,最终变成白色粉末为碳酸钠;
D.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水是复分解反应;
解答:
解:A.因钠很活泼,易被氧化,则金属钠在空气中易氧化形成氧化钠,出现变暗现象,故A正确;
B.氧化钠与空气中的水反应生成氢氧化钠,氢氧化钠吸收空气中的水蒸气在表面形成了溶液,可观察到“出汗”,故B正确;
C.生成的氢氧化钠再与空气中的二氧化碳反应生成碳酸钠的结晶水合物,最终风化变成白色粉末为碳酸钠,故C正确;
D.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水是复分解反应,不是化合反应,故D错误;
故选D.
B.氧化钠与空气中的水反应生成氢氧化钠,氢氧化钠吸收空气中的水蒸气在表面形成了溶液,可观察到“出汗”,故B正确;
C.生成的氢氧化钠再与空气中的二氧化碳反应生成碳酸钠的结晶水合物,最终风化变成白色粉末为碳酸钠,故C正确;
D.氢氧化钠再与空气中的二氧化碳反应生成碳酸钠和水是复分解反应,不是化合反应,故D错误;
故选D.
点评:本题考查钠在空气中的一系列变化,明确钠及其化合物的性质是解答本题的关键,注意发生的化学反应及氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
汽车尾气(含有烃类、CO、NOx、SO2)是城市空气的主要污染源,治理方法之一是在汽车排气管上加装“催化转化器”,它使CO和NOx反应生成可参与大气生态环境循环的无毒气体,并使烃类充分燃烧及SO2转化,下列说法错误的是( )
| A、CO和NOx反应的化学方程式为:2xCO+2NOx=2xCO2+N2 |
| B、上述方法的缺点是由于CO2增多,会大大提高空气的酸度 |
| C、多植树造林,增大绿化面积,可有效控制城市空气各种污染源 |
| D、汽车改用天然气为燃料或开发氢能源,都会减少对空气的污染 |
在10mL0.01mol/L的纯碱溶液中,不断搅拌并逐滴加入1.2mL 0.05mol/L盐酸,完全反应后在标准状况下生成二氧化碳的体积为( )
| A、0mL |
| B、0.672mL |
| C、1.34mL |
| D、2.240mL |
下列物质分类正确的是( )
| A、SO2、CO2、CO均为酸性氧化物 |
| B、稀豆浆、硅酸、氯化铁溶液均为胶体 |
| C、烧碱、纯醋酸、四氯化碳均为电解质 |
| D、空气、混凝土、氨水均为混合物 |
下列离子方程式书写正确的是( )
| A、澄清的石灰水与醋酸反应:OH-+CH3COOH=CH3COO-+H2O |
| B、碳酸钙与盐酸反应:CO2-3+2H+═CO2↑+H2O |
| C、钠与水反应:Na++H2O═Na++OH-+H2↑ |
| D、铜片与硝酸银溶液反应:Cu+Ag+═Cu2++Ag |
铅笔芯的主要成分是石墨.如果铅笔芯写一个字消耗的石墨质量约为1×10-3g,那么一个铅笔字含有的碳原子数约为( )
| A、5×1019个 |
| B、5×1022个 |
| C、2.5×1022个 |
| D、2.5×1019个 |
 :
: :
: :
: :
: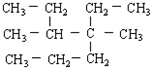 的正确系统命名为
的正确系统命名为