题目内容
将CoCl2溶解于盐酸中可以形成CoCl,在溶液中存在下面的化学平衡:
Co2+(aq)+4Cl-(aq) CoCl(aq) ΔH>0
CoCl(aq) ΔH>0
粉红色 蓝色
下列说法正确的是 ( )
Co2+(aq)+4Cl-(aq)
 CoCl(aq) ΔH>0
CoCl(aq) ΔH>0粉红色 蓝色
下列说法正确的是 ( )
| A.将盛有CoCl2和盐酸混合液的试管置于热水中,试管内溶液为红色 |
| B.升高温度,正反应速率增大,逆反应速率减小 |
| C.该反应的平衡常数K= |
| D.增大Cl-浓度,平衡向正反应方向移动,试管内溶液变为蓝色 |
CD
反应是吸热反应,所以升高温度平衡向正反应方向移动,溶液显蓝色,A不正确。升高温度反应速率都是增大,B不正确。平衡常数是在一定条件下,可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此选项C正确。增大反应物的浓度,平衡向正反应方向移动,溶液显蓝色,D正确。答案选CD。

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
 3C(g) + D(s),反应达到平衡时C的浓度为1.2 mol/L。
3C(g) + D(s),反应达到平衡时C的浓度为1.2 mol/L。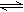 xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是( )
xM(g)+2N(g),5min后达到平衡生成1mol N,经测定这5min内 M的平均速率是0.1mol/(L·min),下列叙述错误的是( ) Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体
Fe(SCN)3(aq)+3KCl(aq),加入KCl晶体 2SO3(g),加入N2
2SO3(g),加入N2 N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。
N2O4(g)。如下图1所示,烧瓶A、B中装有相同浓度的NO2和N2O4的混合气体,中间用止水夹K夹紧,烧杯甲、乙分别盛放100mL冷水和热水。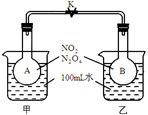
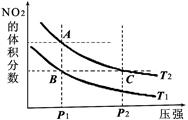
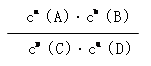
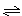 pC(g)+qD(g)中K=
pC(g)+qD(g)中K= 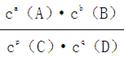
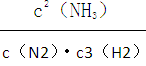
 2NO2(g),不能说明该反应已达到平衡状态的是
2NO2(g),不能说明该反应已达到平衡状态的是 2NH3 (g) △H1
2NH3 (g) △H1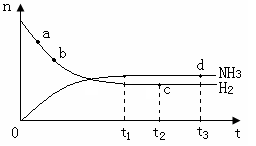
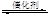 CH3OCH3(g)+3H2O(g) △H<0
CH3OCH3(g)+3H2O(g) △H<0 ?CO2(g)+NO(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ;
?CO2(g)+NO(g)反应过程中能量变化示意图。一定条件下,在固定容积的密闭容器中该反应达到平衡状态。当改变其中一个条件X,Y随X的变化关系曲线如图Ⅱ;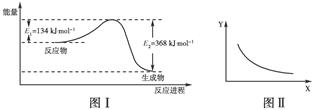
 CO2+H2,达到平衡后,测得CO2为0.6mol,再通入0.4mol水蒸气,又达到平衡后,CO2的物质的量为
CO2+H2,达到平衡后,测得CO2为0.6mol,再通入0.4mol水蒸气,又达到平衡后,CO2的物质的量为