题目内容
在一定温度下,向容积不变的容器中加入2 mol N2、8 mol H 2 及固体催化剂,使之反应.已知:N2(g)+3H2(g)
2 及固体催化剂,使之反应.已知:N2(g)+3H2(g)  2NH3(g);△H="-92.2" kJ·mol-1.平衡时,容器内气体压强为起始时的80%.
2NH3(g);△H="-92.2" kJ·mol-1.平衡时,容器内气体压强为起始时的80%.
(1)反应达到平衡时,放出的热量_______.
A.小于92.2 kJ B.等于92.2 kJ C.大于92.2 kJ
(2)欲使H2的转化率提高为原来的两倍,则在其他条件不变的情况下,应将N2的初始量由2mol提高至__________mol.
(3)保持同一温度,在相同的容器中,若起始时加入2molNH3、1molH2 及固体催化剂,反应达到平衡时NH3的体积分数_________.
A.等于0.25 B.大于0.25 C.小于0.25
(4)右图是T1℃时容器中NH3的物质的量随时间的变化曲线,请在该图中补画出该反应在T2℃(T2>T1)时n(NH3)的变化曲线.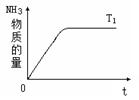
(1)B (2)64.5 (3)C (4)略
解析

练习册系列答案
相关题目
在一定温度下,向容积为2L的密闭容器中充入一定量的CO和NO2发生反应:4CO(g)+2NO2(g)?N2(g)+4CO2(g)△H<0.有关该反应的描述正确的是( )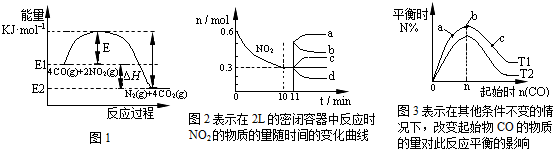

| A、在一定温度、固定容积的密闭容器里,混合气体的密度不再改变可以说明上述可逆反应已达平衡 | B、由图1可得加入适当的催化剂,E和△H都减小 | C、图2中0~10min内该反应的平均速率v(CO)=0.03mol?L-1?min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(NO2)的变化曲线为d | D、图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |