题目内容
4.(1)当胃发生病变时,会出现很多症状,如胃部疼痛等.如果只是由于胃酸过多引起的,则可使用抗酸药进行治疗.现有一种抗酸药的有效成是Mg(OH)2,试写出这种物质与胃酸(以HCl表示)作用的化学方程式Mg(OH)2+2HCl=MgCl2+2H2O.(2)有一种抗酸药,其有效成分是CaCO3,为测定每一片药片中CaCO3的含量,现取一片药片,研成粉末,再与足量盐酸反应,收集到标准状况下的CO2气体22.4mL.则
①CaCO3与足量盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+CO2↑+H2O;
②每一片药片中CaCO3的质量为0.1g.
分析 (1)Mg(OH)2能与盐酸反应生成氯化镁和水;
(2)①碳酸钙与盐酸反应生成氯化钙、水、二氧化碳;
②根据化学方程式进行计算.
解答 解:(1)Mg(OH)2能与盐酸反应生成氯化镁和水:Mg(OH)2+2HCl=MgCl2+2H2O,故答案为:Mg(OH)2+2HCl=MgCl2+2H2O;
(2)①CaCO3与足量盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
②设一片药片中CaCO3的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 22.4L
x 0.0224L
$\frac{100}{x}$=$\frac{22.4L}{0.0224L}$,
解得x=0.1g,
故答案为:0.1.
点评 本题考查抗酸药,题目难度不大,注意碳酸盐与胃酸反应产生二氧化碳气体,可能加重胃溃疡病.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
9. 北斗卫星导航系统是中国自行研制的全球卫星定位与通信系统.发射北斗卫星的火箭推进器中的反应方程式为C2H8N2+2N2O4═2CO2+3N2+4H2O.其中N2O4是( )
北斗卫星导航系统是中国自行研制的全球卫星定位与通信系统.发射北斗卫星的火箭推进器中的反应方程式为C2H8N2+2N2O4═2CO2+3N2+4H2O.其中N2O4是( )
 北斗卫星导航系统是中国自行研制的全球卫星定位与通信系统.发射北斗卫星的火箭推进器中的反应方程式为C2H8N2+2N2O4═2CO2+3N2+4H2O.其中N2O4是( )
北斗卫星导航系统是中国自行研制的全球卫星定位与通信系统.发射北斗卫星的火箭推进器中的反应方程式为C2H8N2+2N2O4═2CO2+3N2+4H2O.其中N2O4是( )| A. | 既是氧化剂又是还原剂 | B. | 还原剂 | ||
| C. | 既不是氧化剂又不是还原剂 | D. | 氧化剂 |
12.以下选项中的两种元素肯定属于同一主族的是( )
| A. | 3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 | |
| B. | 3p轨道上有1个空轨道的原子和4p轨道上有1空轨道的原子 | |
| C. | 最外层电子只有两个电子的甲原子和最外层电子只有两个电子的乙原子 | |
| D. | 最外层电子排布为3s1的原子和最外层电子排布为4s1的原子 |
9.下列四种稀硫酸溶液,均能跟铁片反应,其中最初反应速率最快的是( )
| A. | 常温下 5mL 3mol/L的硫酸溶液 | B. | 标况下10mL 3mol/L的硫酸溶液 | ||
| C. | 标况下 20mL 2mol/L的硫酸溶液 | D. | 常温下300mL 2mol/L的硫酸溶液 |
16.下列物质在空气中存放,不会变质的是( )
| A. | 漂白粉 | B. | 过氧化钠 | C. | 氯水 | D. | 硫酸钠 |
14.下列过程中化学键未被破坏的是( )
| A. | NaCl固体溶于水 | B. | Br2与H2生成HBr | C. | SO2气体溶于水 | D. | 干冰升华 |
 有如图装置:回答下列问题:
有如图装置:回答下列问题: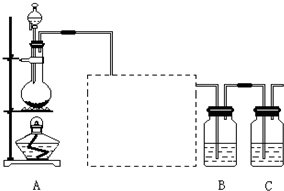
 (1)相对分子质量为72的烷烃,其分子式为C5H12.若此有机物的一氯代物只有一种,请写出此烷烃的结构简式(CH3)4C.
(1)相对分子质量为72的烷烃,其分子式为C5H12.若此有机物的一氯代物只有一种,请写出此烷烃的结构简式(CH3)4C.