题目内容
9.如图是自然界中氮循环的一部分,其中A、B、C为中学化学中常见的化合物.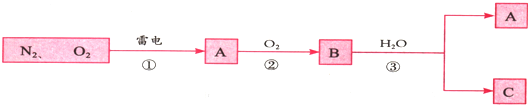
请回答下列问题:
(1)反应②的化学方程式为2NO+O2=2NO2.
(2)反应③的氧化剂为NO2(填序号);
(3)汽车尾气是空气污染源之一,治理的一种方法是用催化剂使尾气中的NO与CO反应生成CO2和N2,该反应中生成1molN2时,被还原的NO为2mol.
分析 空气中的N2在放电条件下与O2直接化合生成无色且不溶于水的一氧化氮气体,N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;常温下就易与空气中的O2反应生成红棕色的二氧化氮气体,2NO+O2=2NO2;二氧化氮气体有毒,易与水反应生成硝酸(HN03)和一氧化氮,3NO2+H2O=2HNO3+NO.
(1)反应②为一氧化氮和氧气的反应;
(2)反应③为二氧化氮和水反应,氧化剂为元素化合价降低的反应物;
(3)NO与CO反应2NO+2CO=2CO2+N2中,NO是氧化剂,被还原,根据方程式计算被还原的NO.
解答 解:(1)反应②为一氧化氮和氧气反应,一氧化氮和氧气化合为二氧化氮,反应为2NO+O2=2NO2,故答案为:2NO+O2=2NO2;
(2)反应③为二氧化氮和水反应,3NO2+H2O=2HNO3+NO,化合价降低N元素所在的反应物NO2是氧化剂,故答案为:NO2;
(3)NO与CO反应生成CO2和N2,反应为:2NO+2CO=2CO2+N2,反应中NO是氧化剂(N化合价+2→0),被还原,生成氮气1mol,被还原的NO为2mol,故答案为:2.
点评 本题考查了氮及其化合物的性质、氧化还原反应的计算,掌握物质的性质和反应原理是关键,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.下列溶液一定呈中性的是( )
| A. | 室温时将pH=5的盐酸稀释100倍所得到的溶液 | |
| B. | 等物质的量的强酸和强碱反应后所得到的混合溶液 | |
| C. | 氢氧化钠溶液与醋酸溶液混合后c(Na+)=c(CH3COO-)的溶液 | |
| D. | 硝酸铵溶于水得到的溶液 |
17.现有100mL 0.1mol/L NaCl 溶液,从中取出10mL,此10mL NaCl 溶液的物质的量浓度为( )
| A. | 0.1mol/L | B. | 0.01mol/L | C. | 0.001mol/L | D. | 无法确定 |
4.下列关于材料的说法正确的是( )
| A. | 水泥是常见的硅酸盐产品 | B. | 光导纤维的主要成分是二氧化硅 | ||
| C. | 蚕丝的主要成分是纤维素 | D. | 合金中一定只含金属元素 |
14.下列事故处理方法正确的是( )
| A. | 实验室钠着火时,立即用水灭火 | |
| B. | 不慎洒出的酒精在桌上着火时,应立即用大量水扑灭 | |
| C. | 浓 NaOH 溶液溅到皮肤上,立即用水冲洗,然后涂上稀硼酸溶液 | |
| D. | 浓硫酸溅到皮肤上,立即用稀 NaOH 溶液洗涤 |
18.下列关于有机化合物的说法正确的是( )
| A. | 1mol苯中含有碳碳双键的数目为3NA | |
| B. | 甲烷、乙烯和苯都可以与溴水发生反应 | |
| C. | 乙烯可以与氢气发生加成反应,苯不能与氢气加成 | |
| D. | CH3-CH=CH-CH3分子中最多有8个原子在同一平面内 |
19.在密闭容器中加入P、Q进行反应P(g)+2Q(g)?2R(g)+S(g),下列说法可以充分说明在恒温下已达到平衡的是( )
| A. | 反应容器中压强不随时间变化而变化 | |
| B. | 反应容器中P、Q、R、S四者共存 | |
| C. | P和S的生成速率相等 | |
| D. | 反应容器中总的物质的量保持不变 |