题目内容
14.求下列粒子的物质的量(1)6.02×1023个SO3中电子的物质的量40mol.
(2)含有6.02×1023个O原子的H2SO4的物质的量0.25mol.
(3)含有6.02×1023个Fe3+的Fe2(SO4)3中SO42-的物质的量1.5mol.
(4)含有6.02×1023个e-的H2O的物质的量0.1mol.
分析 (1)1mol的SO3中电子的物质的量40mol;
(2)先根据n=$\frac{N}{{N}_{A}}$计算O原子的物质的量,再根据化学式可知n(H2SO4)=$\frac{1}{4}$n(O),据此计算;
(3)根据n=$\frac{N}{{N}_{A}}$计算Fe3+的物质的量,由化学式可知n(SO42-)=$\frac{3}{2}$n(Fe3+);
(4)根据n=$\frac{N}{{N}_{A}}$计算电子的物质的量,每个H2O分子含有10个电子,进而计算H2Or的物质的量.
解答 解:(1)1mol的SO3中电子的物质的量40mol,6.02×1023个SO3,三氧化硫的物质的量为1mol,所以6.02×1023个SO3中电子的物质的量为40mol,故答案为:40mol;
(2)6.02×1023个O原子的物质的量n(O)=$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,故n(H2SO4)=$\frac{1}{4}$n(O)=$\frac{1}{4}$×1mol=0.25mol,故答案为:0.25mol;
(3)Fe3+的物质的量为$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,由化学式可知n(SO42-)=$\frac{3}{2}$n(Fe3+)=1mol×$\frac{3}{2}$=1.5mol,故答案为:1.5mol;
(4)电子的物质的量为$\frac{6.02×1{0}^{23}}{6.02×1{0}^{23}mo{l}^{-1}}$=1mol,每个水分子含有10个电子,水物质的量为$\frac{1mol}{10}$=0.1mol,故答案为:0.1mol.
点评 本题考查物质的量有关计算,侧重对微粒数目的计算,比较基础,注意理解掌握微粒构成.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案| A. | K+、Na+、OH-、NO3- | B. | Cu2+、Ba2+、Cl-、NO3- | ||
| C. | Na+、Mg2+、OH-、SO42- | D. | Fe2+、H+、NO3-、ClO- |
| A. | 浓H2SO4、NaOH-腐蚀品 | B. | 酒精-易燃气体 | ||
| C. | KMnO4-氧化剂 | D. | 白磷-易燃固体 |
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
| A. | 纯净物 | B. | 混合物 | C. | 单质 | D. | 不能确定 |
| A. | 集中处理废旧电池,以防止重金属污染环境 | |
| B. | 海产品中加入大量甲醛以延长保鲜期 | |
| C. | 食用蔬菜水果可以补充人体所需维生素 | |
| D. | 使用加碘盐,可预防因缺碘引起的甲状腺肿大 |

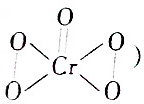 )
)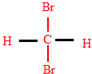 和
和