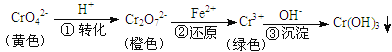题目内容
【题目】A、B、C、X、Y、Z、E为前四周期元素,且原子序数依次增大。A原子核外有三个能级,且每个能级上的电子数相等,C原子成对电子数是未成对电子数的3倍,X、Y、Z、E是位于同一周期的金属元素,X、E原子的最外层电子数均为1,Y有“生物金属”之称,Y4+和氩原子的核外电子排布相同,Z原子核外电子的运动状态数目是最外层电子数的14倍。用元素符号回答下列问题:
(1)B的电子排布式:_____________,Y的价电子排布图____________,Z2+的价电子排布式____________。
(2)E元素位于周期表第________周期__________族_________区。
(3)①A、B、C三种元素的第一电离能由小到大的顺序为_____________。
②A、C元素气态氢化物的稳定性的大小_________>________(分子式表示)原因_____________。
③与AC32-互为等电子体的离子_______(写一种),写出与ABC-离子互为等电子体的分子的化学式:______(写一种)。
④AC2的电子式___________。
【答案】1s22s22p3 ![]() 3d8 四 IB ds C<O<N H2O CH4 氧元素的非金属性强于碳或氧的原子半径比碳原子半径小,键长越小键能越大越稳定 NO3- N2O或CO2
3d8 四 IB ds C<O<N H2O CH4 氧元素的非金属性强于碳或氧的原子半径比碳原子半径小,键长越小键能越大越稳定 NO3- N2O或CO2 ![]()
【解析】
A、B、C、X、Y、Z、E为前四周期元素,且原子序数依次增大。A原子核外有三个能级,且每个能级上的电子数相等,A原子核外电子排布为1s22s22p2,则A为碳元素。X、Y、Z、E是位于同一周期的金属元素,元素只能处于第四周期,Y有“生物金属”之称,Y4+和氩原子的核外电子排布相同,Y元素原子核外电子数=18+4=22,故Y为Ti元素;X原子的最外层电子数为1,且X的原子序数小于Ti,故X为K元素;Z原子核外电子的运动状态数目是最外层电子数的14倍,最外层电子数只能为2,故Z原子核外电子数为28,则Z为Ni元素;E原子的最外层电子数为1,原子序数又大于Ni,则E原子的价电子排布式为3d104s1,则E为Cu元素;C原子成对电子数是未成对电子数的3倍,原子序数又小于X(钾),未成对电子数最大为3,故C原子核外电子排布式为1s22s22p4,则C为O元素;而B的原子序数介于碳、氧之间,所以B为N元素,据此分析解答。
根据上述分析可知A是C,B是N,C是O,X是K,Y是Ti,Z是Ni,E是Cu元素。
(1)B是N元素,原子序数是7,根据构造原理可知N原子的核外电子排布式为:1s22s22p3;Y是22号Ti元素,价电子排布式是3d24s2,价电子排布图为:![]() ;Z是Ni,Ni原子失去最外层的2个电子变为Ni2+,Ni2+的价电子排布式3d8;
;Z是Ni,Ni原子失去最外层的2个电子变为Ni2+,Ni2+的价电子排布式3d8;
(2)E是Cu,原子核外电子排布式是1s22s22p63s23p63d104s1,在元素周期表中位于第四周期第IB族,属于ds区;
(3)①A是C,B是N,C是O,一般情况下,同一周期的元素,随原子序数的增大,元素的第一电离能呈增大趋势,但由于N原子的2p电子处于半充满的稳定状态,所以其第一电离能比O大,则三种元素的第一电离能由小到大的顺序为C<O<N;
②元素的非金属性越强,其相应的简单氢化物的稳定性就越强,由于元素的非金属性C<O,原子半径r(C)>r(O),所以这两种元素的相应氢化物的稳定性:H2O>CH4;
③AC32-离子为CO32-,与其互为等电子体的离子为NO3-;ABC-离子为CNO-,与其互为等电子体的分子的化学式为N2O或CO2。
④AC2是CO2,在该物质分子中,C原子与2个O原子形成四对共用电子对,使分子中每个原子都达到最外层8个电子的稳定结构,所以CO2的电子式为:![]() 。
。

【题目】用中和滴定法测定某烧碱样品的纯度,试根据实验回答下列问题:
(1)准确称量8.2 g含有少量中性易溶杂质的样品,配成500 mL待测溶液。称量时,样品可放在________(填字母)称量。
A.小烧杯中 B.洁净纸片上 C.托盘上
(2)滴定过程中,眼睛应注视________________。滴定时,用0.2000molL-的盐酸来滴定待测液,不可选用______(填编号字母)作指示剂。
A.甲基橙 B.石蕊 C.酚酞
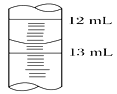
(3)滴定时,用0.200 0 mol·L-1的盐酸来滴定待测溶液,根据下表数据,计算被测烧碱溶液的物质的量浓度是________ mol·L-1,烧碱样品的纯度是________。
滴定次数 | 待测溶液体积(mL) | 标准酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(4)下列实验操作会对滴定结果产生什么后果?(填“偏高”、“偏低”或“无影响”)
①若将锥形瓶用待测液润洗,然后加入10.00mL待测液,则滴定结果______
②若锥形瓶未干燥就加入10.00mL待测液,则滴定结果______。