��Ŀ����
��ɫ����N2O4��һ��ǿ��������Ϊ��Ҫ�Ļ���ƽ���֮һ��N2O4��NO2ת�����Ȼ�ѧ����ʽΪ��N2O4(g)  2 NO2(g) ��H=+24.4 kJ/mol
2 NO2(g) ��H=+24.4 kJ/mol
(1)��һ����N2O4Ͷ��̶��ݻ�����������У�����������˵����Ӧ�ﵽƽ�����_________________��
a��v��(N2O4)=2 v��(NO2) b����ϵ��ɫ����
c������ƽ����Է����������� d�������ܶȲ���
�ﵽƽ�����������������¶ȣ��ٴε���ƽ��ʱ������������ɫ________(�� �����������dz�����䡱)��
(2)ƽ�ⳣ��K���÷�Ӧ��ϵ���������ʷ�ѹ��ʾ����K����ʽ����ƽ���ѹ����ƽ��Ũ�ȣ���ѹ=��ѹ�����ʵ�������(���磺p(NO2)=p�ܡ�x(NO2)��д��������Ӧƽ�ⳣ��Kp����ʽ________________(��p�ܡ����������ʵ�������x��ʾ)��Ӱ��Kp��������____________________��
(3)������Ӧ�У�����Ӧ����v��=k����p(N2O4)���淴Ӧ����v��=k�桤p 2(NO2)������k����k��Ϊ���ʳ�������KpΪ_________(��k����k���ʾ)������һ����N2O4Ͷ����������к��º�ѹ�ֽ�(�¶�298 K��ѹǿ100 kPa)����֪��������k��=4.8��l04 s-1 ����N2O4�ֽ�10%ʱ��v��=___________kPa��s-1��
(4)����ܱ������з���һ����N2O4��ά����ѹǿp0�㶨�����¶�ΪTʱ��ƽ��ʱN2O4�ֽ�ٷ���Ϊa�������¶Ȳ��䣬���ܱ������г������N2O4��ά����ѹǿ��2p0�����·ֽ⣬��N2O4��ƽ��ֽ��ʵı���ʽΪ_______________________��
 �ŵ������ϵ�д�
�ŵ������ϵ�д� 53������ϵ�д�
53������ϵ�д�


 CO(g)+3H2(g) ��H>0����1.0molCH4��2.0molH2Oͨ�˷�Ӧ��1(�����ݻ�Ϊ100L)��10minĩ��0.1molCO���ɣ���10min�ڷ�Ӧ��ƽ������V(H2)=________���÷�Ӧƽ�ⳣ���ı���ʽ��_____________��
CO(g)+3H2(g) ��H>0����1.0molCH4��2.0molH2Oͨ�˷�Ӧ��1(�����ݻ�Ϊ100L)��10minĩ��0.1molCO���ɣ���10min�ڷ�Ӧ��ƽ������V(H2)=________���÷�Ӧƽ�ⳣ���ı���ʽ��_____________��
 CH3OH(g)���Դ˷�Ӧ���������о���
CH3OH(g)���Դ˷�Ӧ���������о��� ���õ�ⷨ�Ʊ��ߴ��ȵ���(��֪��������Fe2����Ni2����Cu2��)������������ȷ����( )
���õ�ⷨ�Ʊ��ߴ��ȵ���(��֪��������Fe2����Ni2����Cu2��)������������ȷ����( )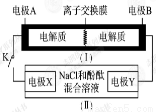
 H2����Cl2����2OH��
H2����Cl2����2OH��