题目内容
某同学在研究前18号元素时发现,可以将它们排成如图所示的“蜗牛”形状,图中每个“ · ”代表一种元素,其中O点代表氢元素.下列说法中错误的是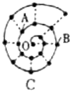
A.离O点越远的元素原子半径越大
B.虚线相连的元素处于同一族,A元素位于元素周期表ⅥA族
C.B元素是图中金属性最强的元素
D.B、C最高价氧化物的水化物可以相互反应
A
解析试题分析:A.离O点越远的元素,原子序数增大,但是若是同一周期的元素,则原子序数越大,原子半径就越小,错误;B.虚线相连的元素处于同一族,A元素是O元素,位于元素周期表ⅥA族,,正确;C.B元素是Na元素,是图中所有短周期元素中金属性最强的元素,正确;D.B、C最高价氧化物的水化物NaOH是强碱,而Al(OH)3是两性氢氧化物,二者可以相互反应,正确。
考点:考查“蜗牛”形状的元素周期表中元素的原子结构与元素的性质的关系的知识。

练习册系列答案
相关题目
几种短周期元素的原子半径和主要化合价见下表,下列说法中正确的是( )。
| 元素代号 | 原子半径/nm | 主要化合价 |
| X | 0.160 | +2 |
| Y | 0.143 | +3 |
| Z | 0.102 | +6、-2 |
| L | 0.099 | +7、-1 |
| M | 0.077 | +4、-4 |
| Q | 0.074 | -2 |
B.Y与Q形成的化合物不能跟氢氧化钠溶液反应
C.Z的氢化物的稳定性强于L的氢化物的稳定性
D.在化学反应中,M原子与其他原子易形成共价键而不易形成离子键
下列微粒:①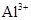 ;②
;②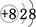 ;③
;③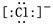 ;④
;④ 。其中核外电子数相同的是( )
。其中核外电子数相同的是( )
| A.①②③ | B.②③④ | C.①②④ | D.①③④ |
已知X、Y、Z都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,则下列说法错误的是 ( )
| A.Y和Z可以组成一种Y和Z的质量比为7:8的化合物 |
| B.X、Y、Z三种元素可以组成一种盐 |
| C.X和Z可以组成原子个数比分别为1:1和2:1常温下为液态的两种化合物 |
| D.由X、Y、Z三种元素中的任意两种组成的具有10电子的微粒有2种 |
下列说法正确的是( )
| A.形成离子键的阴阳离子间只存在静电吸引力 |
| B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱 |
| C.第三周期非金属元素含氧酸的酸性从左到右依次增强 |
| D.元素周期律是元素原子核外电子排布周期性变化的结果 |
下列说法正确的是
| A.K能层中不包含p能级 | B.碳原子的电子排布式为1s22p4 |
| C.3p3表示3p能级有三个轨道 | D.同一原子中,2p、3p、4p能级的轨道数依次增加 |
下列分子中,所有原子的最外层均为8电子结构的是
| A.BeCl2 | B.H2S | C.NCl3 | D.SF6 |
下列说法中正确的是
| A.s区都是金属元素 | B.s区都是主族元素 |
| C.稀有气体在ds区 | D.所有非金属元素都在p区 |
已知短周期元素的离子:aA2+、bB+、cC3-、dD- 都具有相同的电子层结构,则下列叙述正确的是
| A.离子半径 C>D>B>A | B.原子序数 D>C>B>A |
| C.原子半径 A>B>D>C | D.单质的还原性 A>B>D>C |