题目内容
下列按电负性减小顺序排列的是( )
| A、N、O、F |
| B、N、P、As |
| C、K、Na、Li |
| D、Cl、O、H |
考点:元素电离能、电负性的含义及应用
专题:
分析:根据元素周期律知识分析,元素周期表中同周期元素从左到右元素的电负性逐渐增强,同主族元素从上到下元素的电负性逐渐减弱.
解答:
解:元素周期表中同周期元素从左到右元素的电负性逐渐增强,同主族元素从上到下元素的电负性逐渐减弱,则
A.N、O、F为同周期元素,电负性逐渐增强,故A错误;
B.N、P、As为同主族元素,电负性逐渐减弱,故B正确;
C.K、Na、Li为同主族元素,电负性逐渐增强,故C错误;
D.O没有最高正价,Cl有最高正价,因此电负性:O>Cl>H,故D错误;
故选B.
A.N、O、F为同周期元素,电负性逐渐增强,故A错误;
B.N、P、As为同主族元素,电负性逐渐减弱,故B正确;
C.K、Na、Li为同主族元素,电负性逐渐增强,故C错误;
D.O没有最高正价,Cl有最高正价,因此电负性:O>Cl>H,故D错误;
故选B.
点评:本题考查元素周期律知识,题目难度不大,本题注意把握元素周期律的递变规律即可解答.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
我国发射的“神舟五号”载人飞船的燃料是铝粉与高氯酸铵的混合物.点燃时,铝粉氧化放热引发高氯酸铵反应2NH4ClO4=N2↑+4H2O+Cl2↑+O2↑;△H<0.关于该反应叙述不正确的是( )
| A、该反应属于分解反应、氧化还原反应、放热反应 |
| B、该反应瞬间能产生大量高温气体,推动飞船飞行 |
| C、从能量变化上看,该反应是化学能转变为热能和动能 |
| D、反应中NH4ClO4只起到氧化剂的作用 |
aXn-和bYm+两种简单离子,其电子层结构相同,下列关系式或化学式正确( )
| A、a-n=b+m |
| B、a+m=b-n |
| C、氧化物为YOm |
| D、氢化物为HnY或YHn |
下列离子方程式正确的是( )
A、甘氨酸与氢氧化钠溶液反应: | ||
| B、软脂酸与氢氧化钠溶液反应:H++OH-=H2O | ||
C、二氧化碳通入苯酚钠溶液中:CO2+2C6H5O-+H2O→2C6H5OH+CO
| ||
| D、乙酸乙酯与氢氧化钠溶液反应:CH3COOC2H5+OH-→CH3COOH+C2H5O- |
某碱金属0.195g与足量水反应时,生成0.005g氢气,这种金属是( )
| A、Li | B、Na | C、K | D、Rb |
下列过程需要增大反应速率的是( )
| A、钢铁的腐蚀 |
| B、工业上炼铁 |
| C、塑料的老化 |
| D、食物的腐败 |
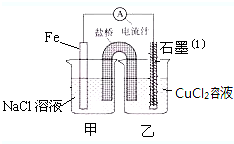 某实验小组的同学对电化学原理进行了一系列探究活动
某实验小组的同学对电化学原理进行了一系列探究活动 氮氧化物和SO2是造成雾霾天气的主要原因之一.
氮氧化物和SO2是造成雾霾天气的主要原因之一.