题目内容
19.在加热氯酸钾的分解反应中,二氧化锰作催化剂的问题,到目前还没有肯定的解释.鉴于反应制得氧气中有氯气的气味,生成的氯化钾又带有紫红色,认为反应过程如下:①2KClO3+2MnO2$\frac{\underline{\;△\;}}{\;}$2A+B↑+C↑ ②2A$\frac{\underline{\;△\;}}{\;}$D+MnO2+C↑ ③B+D$\frac{\underline{\;△\;}}{\;}$2KCl+MnO2+C↑
(1)写出A、B、C、D的化学式:AKMnO4,BCl2,CO2,DK2MnO4.
(2)第①步反应中,氧化产物是(填化学式)KMnO4、O2,被还原的元素是(填元素号)Cl.
(3)第③步反应的化学方程式为Cl2+K2MnO4═2KCl+MnO2+O2↑.
分析 由质量守恒定律及发生的反应,利用反应②可知A为KMnO4,D为K2MnO4,C为气体应为O2,B为气体,则B为Cl2,
则①2KClO3+2MnO2$\frac{\underline{\;\;△\;\;}}{\;}$2KMnO4+Cl2↑+O2↑
②2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
③Cl2+K2MnO4$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+MnO2+O2↑
(1)根据以上分析写出化学式;
(2)反应①中Cl元素的化合价降低,O、Mn元素的化合价升高;
(3)由上述分析可知第③步反应的化学方程式.
解答 解:由质量守恒定律及发生的反应,利用反应②可知A为KMnO4,D为K2MnO4,C为气体应为O2,B为气体,则B为Cl2,
则①2KClO3+2MnO2$\frac{\underline{\;\;△\;\;}}{\;}$2KMnO4+Cl2↑+O2↑
②2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
③Cl2+K2MnO4$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+MnO2+O2↑
(1)A为KMnO4,D为K2MnO4,C为气体应为O2,B为气体,则B为Cl2;
故答案为:KMnO4;Cl2;O2;K2MnO4;
(2)反应①中Cl元素的化合价降低,被还原,O、Mn元素的化合价升高被氧化,KMnO4、O2为氧化产物,
故答案为:KMnO4、O2;Cl;
(3)由上述分析可知发生的反应为Cl2+K2MnO4═2KCl+MnO2+O2↑,
故答案为:Cl2+K2MnO4═2KCl+MnO2+O2↑.
点评 本题考查氧化还原反应,把握质量守恒定律及反应中元素的化合价变化为解答的关键,侧重反应机理的考查,注意从守恒的角度推断物质及判断元素的化合价,题目难度不大.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 2:1 | B. | 1:21 | C. | 3:1 | D. | 以上都不正确 |
| A. | CO2通入Na2SiO3溶液中可以得到硅酸 | |
| B. | 因为高温时SiO2与Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 | |
| C. | SiO2是酸性氧化物,它不溶于水也水溶于任何酸 | |
| D. | 在制玻璃、制水泥的工业生产中,都需要的原料之一是纯碱 |
| A. | 水 | B. | NaOH溶液 | C. | 饱和食盐水 | D. | 石灰水 |
| 实验Ⅰ | 实验Ⅱ | 实验Ⅲ | |
| 反应温度/℃ | 800 | 800 | 850 |
| c(A)起始/mol•L-1 | 1 | 2 | 1 |
| c(A)平衡/mol•L-1 | 0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
| A. | 实验Ⅲ的化学平衡常数K<1 | |
| B. | 实验放出的热量关系为b=2a | |
| C. | 实验Ⅲ在30 min达到平衡,30 min内A的速率:v(A)=0.002 5 mol•L-1•min-1 | |
| D. | 当容器内气体密度不随时间而变化时上述反应达到平衡 |
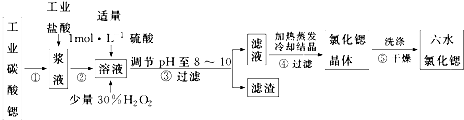
请回答:(1)步骤③中调节溶液pH至8~10,宜选用的试剂为BD.
A.稀硫酸 B.氢氧化锶粉末 C.氢氧化钠 D.氧化锶粉末
所得滤渣的主要成分是BaSO4、Fe(OH)3(填化学式).
(2)若滤液中Ba2+ 浓度为1×10-5mol•L-1,依据下表数据可以推算滤液中Sr2+物质的量浓度为不大于0.03mol/L.
| SrSO4 | BaSO4 | Sr(OH)2 | Fe(OH)3 | Fe(OH)2 | |
| Ksp | 3.3×10-7 | 1.1×10-10 | 3.2×10-4 | 2.6×10-39 | 4.87×10-17 |
| A. | 原子半径:W>Z>Y>X | |
| B. | Y元素在周期表中的位置为第3周期第ⅣA族 | |
| C. | 1 mol甲与足量的乙完全反应共转移1 mol电子 | |
| D. | 化合物甲中只有离子键 |