题目内容
14.由体积为aL的BaCl2和NaCl的混合溶液,将它平均分成两份,一份滴加稀硫酸,使BaCl2恰好完全反应形成沉淀,另一份加入AgNO3溶液至恰好完全反应,经测定,反应中分别消耗xmol的硫酸和ymol的AgNO3溶液至恰好完全反应,经测定,反应中分别消耗xmol的硫酸和ymol的AgNO3.由此可知,原混合溶液中的Na+的物质的量浓度为( )| A. | $\frac{y-2x}{a}$mol•L-1 | B. | $\frac{y-x}{a}$mol•L-1 | C. | $\frac{2(y-x)}{a}$mol•L-1 | D. | $\frac{2(y-2x)}{a}$mol•L-1 |
分析 由BaCl2和稀硫酸反应可计算Ba2+离子的物质的量,利用NaCl和AgNO3溶液反应计算出Cl-离子的物质的量,由混合液呈电中性可计算出钠离子的物质的量,并注意均分成两份及计算原混合溶液中的c(Na+)来解答即可.
解答 解:设每份中的Ba2+离子的物质的量为m,Cl-离子的物质的量为n,
由Ba2++SO42-═BaSO4↓
1 1
m xmol
得:m=xmol,
Cl-+Ag+═AgCl↓
1 1
n ymol
得:n=ymol,
设每份中的钠离子的物质的量为z,BaCl2和NaCl的混合溶液不显电性,
则x×2+z=y,z=(y-2x)mol,则原溶液中的钠离子为(y-2x)mol×2=(2y-4x)mol,
c(Na+)=$\frac{(2y-4x)mol}{aL}$=$\frac{2(y-2x)}{aL}$mol/L,故选D.
点评 本题考查学生利用离子反应方程式的计算,明确离子之间的量的关系即可解答,利用溶液不显电性来计算钠离子的物质的量是解答的关键,并注意两等份的关系,题目难度中等.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
4. 如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应,A、B、C都可以被强还原剂还原成为D(C6H14O6).下面的说法错误的是( )
如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应,A、B、C都可以被强还原剂还原成为D(C6H14O6).下面的说法错误的是( )
 如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应,A、B、C都可以被强还原剂还原成为D(C6H14O6).下面的说法错误的是( )
如图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应,A、B、C都可以被强还原剂还原成为D(C6H14O6).下面的说法错误的是( )| A. | 果糖与A属于同分异构体 | B. | A在酒化酶催化下能产生C2H5OH | ||
| C. | B和C都属于糖类 | D. | D是1,2,3,4,5,6-己六醇 |
2.下列电离方程式正确的是( )
| A. | NaHCO3═Na++H++CO32- | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | H2SO4═H2++SO42- | D. | Ba(OH)2═Ba2++OH- |
9.在下列各组溶液中,离子一定能大量共存的是( )
| A. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、I- | |
| B. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、SiO32-、NO3- | |
| C. | FeCl3溶液:K+、Na+、SO42-、AlO2- | |
| D. | 含0.1mol/LNH4Al(SO4)2的溶液:K+、Ca2+、HCO3-、Cl- |
19.下列粒子对水的电离平衡一定无影响的是( )
| A. | 比例模型为 的某有机分子 的某有机分子 | B. | 某离子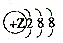 | ||
| C. | ${\;}_{11}^{23}$M+ | D. | 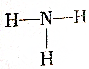 |
6.下列物质中,所含分子数目最多的是( )
| A. | 2g氢气 | B. | 16g氧气 | ||
| C. | 2mol Cl2 | D. | 6.02×1023个氯分子 |




 ,化合物BA2的结构式是:S=C=S;
,化合物BA2的结构式是:S=C=S; .
.