题目内容
6.下列物质中,所含分子数目最多的是( )| A. | 2g氢气 | B. | 16g氧气 | ||
| C. | 2mol Cl2 | D. | 6.02×1023个氯分子 |
分析 由N=nNA可知,物质的量越大,分子数目越多,用题给条件计算各物质的物质的量,比较分子数的多少.
解答 解:A、2g氢气的物质的量为$\frac{2g}{2g/mol}$=1mol,含分子数为NA;
B、16g氧气物质的量=$\frac{16g}{32g/mol}$=0.5mol 即分子数为0.5NA;
C、2mol Cl2,分子数为2NA;
D、6.02×1023个氯分子,即分子数为NA;
故选C.
点评 本题考查了阿伏伽德罗常的应用,重点需要掌握物质的量与质量、微粒数、气体体积的换算关系,题目难度不大.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
16.化学与社会、生活密切相关,下列说法正确的是( )
| A. | 在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放 | |
| B. | 石英、玛瑙、太阳能电池的主要成分均为二氧化硅 | |
| C. | 海水中含有丰富的资源,不经化学反应可从海水中提取溴、镁、氯化钠等物质 | |
| D. | 直馏汽油、裂化汽油、植物油、甘油均能使溴的四氯化碳溶液褪色 |
17.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A. | 78g苯分子中含有碳碳双键数为3NA | |
| B. | 1 mol羟基所含的电子总数为9NA | |
| C. | 常温下,2.24 L乙烷与乙烯混合气体中所含碳原子数为0.2NA | |
| D. | 标准状况下,11.2 L苯所含分子数为0.5 NA |
14.由体积为aL的BaCl2和NaCl的混合溶液,将它平均分成两份,一份滴加稀硫酸,使BaCl2恰好完全反应形成沉淀,另一份加入AgNO3溶液至恰好完全反应,经测定,反应中分别消耗xmol的硫酸和ymol的AgNO3溶液至恰好完全反应,经测定,反应中分别消耗xmol的硫酸和ymol的AgNO3.由此可知,原混合溶液中的Na+的物质的量浓度为( )
| A. | $\frac{y-2x}{a}$mol•L-1 | B. | $\frac{y-x}{a}$mol•L-1 | C. | $\frac{2(y-x)}{a}$mol•L-1 | D. | $\frac{2(y-2x)}{a}$mol•L-1 |
1.下列物质的水溶液导电性最强的是( )
| A. | 0.50mol•L-1 H2SO4溶液 | B. | 0.50mol•L-1 KNO3 溶液 | ||
| C. | 0.50mol•L-1酒精溶液 | D. | 0.50mol•L-1NaOH溶液 |
11. 水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸(
水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
实验步骤:
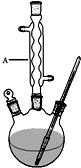
Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g.
常用物理常数:
请根据以上信息回答下列问题:
(1)仪器A的名称是球形冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)反应结束后,分离甲醇的操作是蒸馏(或水洗分液).
(3)洗涤操作中,第一次水洗的主要目的是洗掉大部分的硫酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(4)检验产品中是否含有水杨酸的化学方法是向产品中滴加少量的紫色石蕊试液,观察是否变红.
(5)本实验的产率为59%(保留两位有效数字).
 水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸(
水杨酸甲酯又叫冬青油,是一种重要的有机合成原料.某化学小组用水杨酸( )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率.实验步骤:
Ⅰ.如图,在三颈烧瓶中加入6.9g (0.05mol)水杨酸和24g(30mL,0.75mol)甲醇,向混合物中加入约10mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3 溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯4.5g.
常用物理常数:
| 名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
| 水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
| 水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
| 甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
(1)仪器A的名称是球形冷凝管,制备水杨酸甲酯时,最合适的加热方法是水浴加热.
(2)反应结束后,分离甲醇的操作是蒸馏(或水洗分液).
(3)洗涤操作中,第一次水洗的主要目的是洗掉大部分的硫酸,第二次水洗的主要目的是洗掉碳酸氢钠.
(4)检验产品中是否含有水杨酸的化学方法是向产品中滴加少量的紫色石蕊试液,观察是否变红.
(5)本实验的产率为59%(保留两位有效数字).
12.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=1的溶液中:K+、Fe2+、MnO4-、SO42- | |
| B. | c(Fe3+)=0.1mol•L-1的溶液中:K+、ClO-、SO42-、SCN- | |
| C. | pH=12的溶液中:K+、Na+、Br-、AlO2- | |
| D. | 与铝反应生成H2的溶液中:NH4+、K+、Cl-、SiO32- |