题目内容
19.下列有关乙酸的说法正确的是( )| A. | pH=3的醋酸与pH=11的氢氧化钠溶液等体积混合所得溶液的pH<7 | |
| B. | 反应2CO(g)+2H2(g)→CH3COOH (l)的△S>0 | |
| C. | 冰醋酸用水稀释,溶液中c(H+)先变大后变小 | |
| D. | 含有CH3COOH、C2H5OH、CH3COOC2H5及H2O的平衡体系中加入少量浓硫酸,CH3COOC2H5的物质的量不变 |
分析 A.醋酸为弱酸,在溶液中部分电离,则混合液中醋酸过量,溶液呈酸性;
B.该反应是气体体积缩小的反应,则熵变小于0;
C.冰醋酸为共价化合物,不发生电离,加入水后氢离子浓度增大,随着溶液体积增大,氢离子浓度会逐渐减小;
D.浓硫酸具有吸水性,水的物质的量减小,平衡向着正向移动.
解答 解:A.pH=3的醋酸与pH=11的氢氧化钠溶液等体积混合,醋酸过量,溶液呈酸性,则所得溶液的pH<7,故A正确;
B.反应2CO(g)+2H2(g)→CH3COOH(l)的正反应气体体积缩小,其熵变△S<0,故B错误;
C.冰醋酸用水稀释,开始时溶液中氢离子浓度增大,之后随着溶液体积增大,溶液体积变化较大,则氢离子浓度会逐渐减小,则溶液中c(H+)先变大后变小,故C正确;
D.含有CH3COOH、C2H5OH、CH3COOC2H5及H2O的平衡体系中加入少量浓硫酸,浓硫酸具有吸水性,导致平衡向着正向移动,则CH3COOC2H5的物质的量增大,故D错误;
故选AC.
点评 本题考查了弱电解质的电离平衡及其影响、化学平衡及其影响,题目难度中等,注意掌握弱电解质的电离平衡、化学平衡及其影响因素,C为易错点,注意掌握醋酸的电离特点,试题培养了学生的灵活应用基础知识的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.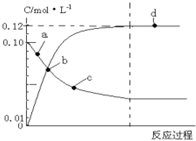 373K时,N2O4(g)?2NO2(g)平衡体系的建立过程中各物质浓度与时间的关系如图,下列说法正确的是( )
373K时,N2O4(g)?2NO2(g)平衡体系的建立过程中各物质浓度与时间的关系如图,下列说法正确的是( )
 373K时,N2O4(g)?2NO2(g)平衡体系的建立过程中各物质浓度与时间的关系如图,下列说法正确的是( )
373K时,N2O4(g)?2NO2(g)平衡体系的建立过程中各物质浓度与时间的关系如图,下列说法正确的是( )| A. | 反应达到a点时,正反应速率大于逆反应速率 | |
| B. | 反应达到b时,表示反应达到平衡 | |
| C. | 反应达到b点时,NO2和 N2O4二者浓度相等 | |
| D. | 反应达到d点时,N2O4的转化率为40% |
10.某实验小组探究工业上废渣(主要成分为Cu2S和Fe2O3)的综合利用,过程如下:
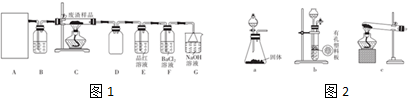
(1)该小组同学设计如图1装置模拟废渣在过量氧气中焙烧,并验证废渣中含有硫元素.
①在实验室中,图2装置可以作为装置A的是ac.
②证明废渣中含有硫元素的实验现象是装置E中品红溶液褪色.
③装置F中生成白色沉淀的离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(2)某同学将上述实验中灼烧后的固体A进行如下操作:
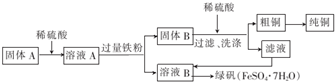
①固体B的成分是Fe、Cu(填化学式).
②由溶液B得到绿矾的过程中应该进行的操作是蒸发浓缩,冷却结晶、过滤、洗涤、干燥.
③为测定产品中绿矾的质量分数,称取30.0g样品配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,反应为10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe(SO4)3+K2SO4+8H2O.实验所得数据如表所示.
Ⅰ.第1组实验数据出现异常,造成这种异常的原因可能是ac(填字母).
a.量取绿矾溶液的酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
Ⅱ.根据表中数据,产品中绿矾的质量分数为92.7%.

(1)该小组同学设计如图1装置模拟废渣在过量氧气中焙烧,并验证废渣中含有硫元素.
①在实验室中,图2装置可以作为装置A的是ac.
②证明废渣中含有硫元素的实验现象是装置E中品红溶液褪色.
③装置F中生成白色沉淀的离子方程式为2SO2+O2+2H2O+2Ba2+=2BaSO4↓+4H+.
(2)某同学将上述实验中灼烧后的固体A进行如下操作:

①固体B的成分是Fe、Cu(填化学式).
②由溶液B得到绿矾的过程中应该进行的操作是蒸发浓缩,冷却结晶、过滤、洗涤、干燥.
③为测定产品中绿矾的质量分数,称取30.0g样品配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.10mol•L-1的酸性KMnO4溶液进行滴定,反应为10FeSO4+8H2SO4+2KMnO4═2MnSO4+5Fe(SO4)3+K2SO4+8H2O.实验所得数据如表所示.
| 滴定次数 | 1 | 2 | 3 | 4 |
| 消耗酸性KMnO4溶液的体积/mL | 19.10 | 20.02 | 19.98 | 20.00 |
a.量取绿矾溶液的酸式滴定管用蒸馏水洗净后未用标准液润洗
b.锥形瓶洗净后未干燥
c.滴定终点时俯视读数
d.滴定前尖嘴有气泡,滴定后气泡消失
Ⅱ.根据表中数据,产品中绿矾的质量分数为92.7%.
7.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. | 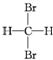 和 和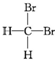 互为同分异构体 互为同分异构体 | ||
| C. | 戊烷有两种同分异构体 | D. | 金刚石与石墨是同素异形体 |
14.下列说法正确的是( )
| A. | 100℃时水的离子积常数Kw为5.5×10-13,说明水的电离是放热反应 | |
| B. | 配制Fe(NO3)2溶液时,为了防止Fe2+水解可向溶液中加入适量的稀硝酸 | |
| C. | NaClO溶液中通入少量CO2,ClO-水解程度增大,溶液碱性增强 | |
| D. | 0.1 mol/L CH3COOH溶液加水稀释后,CH3COOH的电离程度和溶液中c(OH-)都增大 |
4.下表为元素周期表的一部分,其中X、Y、Z、W为短周期元素,X与Y的原子序数之和为Z与W原子序数之和的$\frac{2}{3}$.下列说法正确的是( )
| X | |||
| Y | Z | W | |
| T |
| A. | Mg在一定条件下可以和YX2发生反应生成Y单质 | |
| B. | 化合物YX2、ZX2化学键类型和晶体类型均相同 | |
| C. | Z、W、T三种元素最高价氧化物的水化物的酸性依次增强 | |
| D. | 五种元素中,只有T是金属元素 |
11.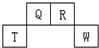 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )
 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )| A. | 原子半径Q>R>T | |
| B. | 原子序数比R多1的元素只能形成一种氢化物 | |
| C. | W原子得电子能力强于Q原子,且可形成共价化合物QW2 | |
| D. | 与W同一主族的下一周期元素不可作为半导体材料 |
8.进行下列反应后,所得溶液中一定只含有一种溶质的是( )
| A. | 将铁粉加到稀硝酸中 | |
| B. | 向稀盐酸中滴入少量的NaAlO2溶液 | |
| C. | 向MgSO4、H2SO4的混合溶液中加入过量的Ba(OH)2溶液 | |
| D. | 室温下,NaOH溶液与醋酸溶液反应后所得的pH大于7的溶液 |
9.下列元素中,非金属性最强的是( )
| A. | S | B. | Mg | C. | P | D. | Cl |