题目内容
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA
B.常温常压下,44 g C3H8中含有的碳碳单键数为3 NA
C.标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数为3 NA
D.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA
D
【解析】
试题分析:A、氯气与水的反应是可逆反应,所以0.1mol的氯气不会完全反应,所以转移电子的物质的量小于0.1mol,电子数则小于0.1NA,错误;B、丙烷的摩尔质量是44g/mol,所以44g丙烷的物质的量是1mol,1个丙烷分子中含有2个碳碳单键,所以1mol丙烷中含有2NA碳碳单键,错误;C、标准状况下44.8LNO气体与22.4L氧气的物质的量分别是2mol、1mol,二者混合后发生化学反应,恰好生成2mol二氧化氮,所以混合后的分子总数是2NA,错误;D、氧化钠中的阳离子是钠离子,阴离子是O2-,过氧化钠中的阳离子也是钠离子,阴离子是O22-,所以阳离子与阴离子的个数比都是2:1,则1mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA,正确,答案选D。
考点:考查阿伏伽德罗常数与微粒数的关系

 中考解读考点精练系列答案
中考解读考点精练系列答案“绿色化学实验”进课堂,某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验。先给钠预热,当钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,生成大量白烟。
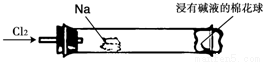
以下叙述错误的是
A.反应生成的大量白烟是氯化钠晶体
B.玻璃管尾部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免污染空气
C.钠着火燃烧产生苍白色火焰
D.棉球外沿滴一滴淀粉碘化钾溶液,可据其颜色变化判断氯气是否被碱液完全吸收
下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
B | NaHCO3为强碱弱酸盐 | NaHCO3 溶液显碱性 |
C | SO2具有氧化性 | SO2可用品红溶液检验 |
D | Fe(OH)3胶体有丁达尔效应 | Fe(OH)3胶体可以用FeCl3浓溶液与NaOH溶液反应制得 |

 2 CH3OCOOC2H5(g) ΔH1
2 CH3OCOOC2H5(g) ΔH1
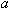 g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是
g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是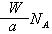 个原子
个原子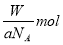 D.由已知信息可得:
D.由已知信息可得: mol-1
mol-1