题目内容
10.化学反应的过程都是旧键断裂、新键形成的过程.对于反应:H2+I2=2HI,已知断开1molH-H键、1molI-I键分别需要吸收的能量是436kJ和151kJ,形成1molH-I键需要放出的能量是299kJ.(1)1molH2和1molI2充分反应,反应物断键吸收的总能量是587kJ,生成物成键放出的总能量为598kJ,该反应属于放热反应(填“放热反应”或“吸热反应”).
(2)如图两个图象中,能够正确反映该反应能量变化的图象是B(填“A”或“B”).
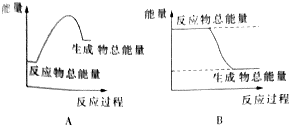
分析 (1)旧键断裂要吸收能量,新键生成要释放能量,当旧键断裂吸收的能量大于新键生成释放的能量时,反应为吸热反应,反之则为放热反应;
(2)由(1)的分析该反应为放热反应,则反应物总能量大于生成物总能量.
解答 解:(1)1mol H2和1mol I2充分反应生成2molHI,旧键断裂吸收能量的值为:436kJ+151kJ=587kJ,新键生成释放能量为:299kJ×2=598kJ,旧键断裂吸收的能量小于新键生成释放的能量,反应为放热反应,放出的热量为:598KJ-587kJ=11kJ,所以放出11kJ,
故答案为:587;598;放热反应;
(2)由(1)的分析该反应为放热反应,则反应物总能量大于生成物总能量,所以B正确;
故选:B.
点评 本题考查了焓变的计算及其与吸放热的图象分析,题目难度不大,注意旧键断裂吸收能量,新键生成释放能量.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
1.下列有机化合物的一氯取代物的同分异构体的数目相等的是( )
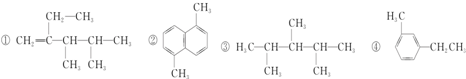

| A. | ①② | B. | ②④ | C. | ③④ | D. | ①④ |
18.按电子排布,可把周期表里的元素划分成5个区,以下元素属于p区的是( )
| A. | Fe | B. | Mg | C. | Br | D. | Cu |
20.下列各项中,表达正确的是( )
| A. | O原子的结构示意图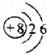 | B. | CH4分子的比例模型 | ||
| C. | C2H2分子的结构式CH≡CH | D. | N2分子的电子式 |
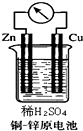 如图所示的铜-锌原电池中,理论上应观察到的现象是:
如图所示的铜-锌原电池中,理论上应观察到的现象是: 工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示
工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示 .有机物X的键线式为
.有机物X的键线式为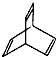
 .
.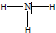 .
.