题目内容
5.某厂的酸性工业废水中含有一定量的Na+、Al3+、Fe3+、Cu2+、Cl-.该厂利用如图所示的工艺流程图,利用常见的气体氧化物、酸、碱和工业生产中的废铁屑,从废水中生产出了氯化铁、氧化铝、NaCl晶体和金属铜,产生了很好的社会经济效益.
请填写下列空白:
(1)图中试剂1是废铁屑,试剂2是稀盐酸.试剂4最好是CO2.
(2)步骤1和步骤2所用到的玻璃仪器是漏斗、玻璃棒、烧杯.
(3)步骤1反应的离子方程式为Fe+Cu2+═Cu+Fe2+,Fe+2Fe3+═3Fe2+,Fe+2H+═Fe2++H2↑.
(4)步骤5反应的离子方程式为AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-.
(5)Al(OH)3可用以下三种途径制备
①Al$\stackrel{NaOH}{→}$NaAlO2$\stackrel{H_{2}SO_{4}}{→}$Al(OH)3②Al$\stackrel{H_{2}SO_{4}}{→}$Al2(SO4)3$\stackrel{NaOH}{→}$Al(OH)3
③

上述三途径制备Al(OH)3你认为最佳途径是③,理由是途径③中反应物的用量便于控制,不会使生成的氢氧化铝溶解,同时消耗的酸碱的量相对较少.
分析 酸性工业废水中含有一定量的Na+、Al3+、Fe3+、Cu2+、Cl-,由工艺流程图示知,溶液A中不含有铜离子,故应加入比铜活泼的金属置换出铜离子,然后把铁离子还原为液态离子,此金属还能与酸反应放出气体,故试剂1为铁屑;金属铜以及多余的铁屑进入沉淀A,然后加入稀盐酸,铁粉溶解生成溶液B,剩余沉淀B为铜粉;溶液A中剩余Na+、Al3+、Fe2+和Cl-,加入过量的氢氧化钠溶液可以使铝离子形成偏铝酸根留在溶液中,亚铁离子沉淀出来,故试剂3为氢氧化钠溶液,偏铝酸盐溶于中通入二氧化碳气体,偏铝酸根变成氢氧化铝沉淀出来,即沉淀D,可以防止氢氧化铝溶液,所以试剂4最好是二氧化碳,最后得NaCl,据此解答各小题即可.
解答 解:酸性工业废水中含有一定量的Na+、Al3+、Fe3+、Cu2+、Cl-,由工艺流程图示知,溶液A中不含有铜离子,故应加入比铜活泼的金属置换出铜离子,然后把铁离子还原为液态离子,此金属还能与酸反应放出气体,故试剂1为铁屑;金属铜以及多余的铁屑进入沉淀A,然后加入稀盐酸,铁粉溶解生成溶液B,剩余沉淀B为铜粉;溶液A中剩余Na+、Al3+、Fe2+和Cl-,加入过量的氢氧化钠溶液可以使铝离子形成偏铝酸根留在溶液中,亚铁离子沉淀出来,故试剂3为氢氧化钠溶液,偏铝酸盐溶于中通入二氧化碳气体,偏铝酸根变成氢氧化铝沉淀出来,即沉淀D,可以防止氢氧化铝溶液,所以试剂4最好是二氧化碳,最后得NaCl,
(1)依据分析可知,图中试剂1是废铁屑,试剂2是稀盐酸,试剂4最好是CO2,
故答案为:废铁屑;稀盐酸;CO2;
(2)步骤1和步骤2均为分离固体和液体操作,即过滤,过滤中使用仪器:漏斗、玻璃棒、烧杯,
故答案为:漏斗、玻璃棒、烧杯;
(3)步骤1中加入的是废铁屑,铁比铜活泼能置换出铜离子,然后把铁离子还原为亚铁离子,Fe还能与酸反应放出气体,有关反应的离子方程式为:Fe+Cu2+═Cu+Fe2+,Fe+2Fe3+═3Fe2+,Fe+2H+═Fe2++H2↑,
故答案为:Fe+Cu2+═Cu+Fe2+,Fe+2Fe3+═3Fe2+,Fe+2H+═Fe2++H2↑;
(4)步骤5为偏铝酸盐溶于中通入二氧化碳气体,偏铝酸根变成氢氧化铝沉淀出来,反应的离子方程式为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-,
故答案为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3-;
(5)比较三种途径中消耗的硫酸和氢氧化钠的量可以知道,途径①②消耗酸、碱的量较多,且不便于控制反应物的量,当酸或碱过量时,氢氧化铝又会溶解,所以最佳途径是③,途径③中反应物的用量便于控制,不会使生成的氢氧化铝溶解,同时消耗的酸碱的量相对较少,
故答案为:③;途径③中反应物的用量便于控制,不会使生成的氢氧化铝溶解,同时消耗的酸碱的量相对较少.
点评 本题主要考查的是从酸液废水中提取金属以及其化合物的流程,涉及:金属活动性顺序、离子反应方程式书写、氢氧化铝的两性等,综合性较强,有一定难度.

| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
| A. | 分子式为H2O和D2O的性质相同 | |
| B. | 相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能 途径a:C$→_{高温}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O 途径b:C$→_{燃烧}^{O_{2}}$CO2 | |
| C. | pM2.5是指大气中直径接近2.5×10-6m的颗粒物,分散在空气中形成胶体 | |
| D. | 氢氧燃料电池的能量转换形式仅为化学能转化为电能. |
(1)人们常用催化剂来选择反应进行的方向,如图1为一定条件下1 molCH3OH与O2发生反应时,生成CO或CO2或HCHO的能量变化[反应物O2(g)和生成物H2O(g)已略去].
①在有催化剂的作用下,CH3OH与O2反应的主要产物是HCHO(填“CO”“CO2”或“HCHO”).
②2HCHO(g)+O2(g)=2CO(g)+2H2O(g)△H=-470KJ•mol-1.
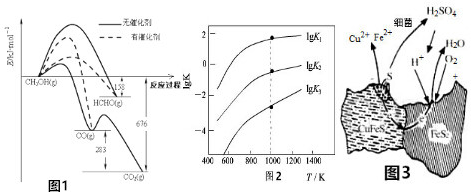
(2)煤炭中的硫主要以黄铁矿的形式存在,用氢气脱出黄铁矿中硫的相关反应见下表,其相关反应的平衡常数的对数值与温度的关系如图2.
| 相关反应 | 反应热 | 平衡常数K |
| ①FeS2(s)+H2(g)?FeS(s)+H2S(g) | △H1 | K1 |
| ②$\frac{1}{2}$FeS2(s)+H2(g)?$\frac{1}{2}$FeS(s)+H2S(g) | △H2 | K2 |
| ③FeS(s)+H2(g)?Fe(s)+H2S(g) | △H3 | K3 |
②提高硫的脱除率可采取的措施有升高温度(任填一种).
③1000K时,向2L恒容密闭容器中充入一定量的H2(g)和FeS2(g),只发生反应①,达到平衡时,H2的转化率为99%.
(3)用细菌冶炼铜时,当黄铜矿中伴有黄铁矿时,可明显提高浸取速率,其原理如图3.
①冶炼过程中,正极周围溶液的pH增大(填“增大”“减小”或“不变”).
②负极产生单质硫的电极反应式为CuFeS2-4e-=Cu2++Fe2++2S.
| A. | 向Na2SiO3溶液中通入过量SO2:SiO32-+SO2+H2O=H2SiO3↓+SO32- | |
| B. | 向NH4HCO3溶液中加过量NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 向Al2(SO4)3溶液中加入过量的NH3•H2O:Al3++4NH3•H2O=[Al(OH)4]-+4NH4+ | |
| D. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O=4Na++2Cu(OH)2↓+O2↑ |
 利用水煤气合成甲醇是煤液化的一种重要方法,其反应的热化学方程式为CO(g)+2H2(g)?CH3OH(l)△H=-90.8kJ•mol-1,在容积为1L的恒容密闭容器中,充入一定量CO和H2,测得CO和H2的物质的量的变化曲线如图所示.
利用水煤气合成甲醇是煤液化的一种重要方法,其反应的热化学方程式为CO(g)+2H2(g)?CH3OH(l)△H=-90.8kJ•mol-1,在容积为1L的恒容密闭容器中,充入一定量CO和H2,测得CO和H2的物质的量的变化曲线如图所示.

 Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).请回答下列问题:
Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料Cl2氧化能力强于H2O2,能将H2O2氧化.为了验证该结论,学生设计了如图所示的实验装置进行实验(夹持装置略去).请回答下列问题: HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑(用化学方程式表示)
HCl+HClO;2HClO$\frac{\underline{\;光照\;}}{\;}$2HCl+O2↑(用化学方程式表示)