题目内容
下列离子方程式表达正确的是( )
| A、HCO3-的水解方程式可表示为:HCO3-+H2O?H3O++CO32- |
| B、向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O |
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)3Fe+8 H++2NO3-=3Fe2++2NO↑+4H2O |
考点:离子方程式的书写
专题:
分析:A.HCO3-的水解生成碳酸和氢氧根离子;
B.向NaHCO3溶液中加入过量的澄清石灰水,反应生成碳酸钙、氢氧化钠和水;
C.二氧化碳过量,反应生成碳酸氢根离子;
D.16.8g 铁粉物质的量=
=0.3mol,100mL 4.0mol/L的HNO3溶液中含硝酸的物质的量=0.1L×4.0mol/L=0.4mol,依据3Fe+8HNO3═3Fe(NO3)2+2NO↑+4H2O,可知铁过量反应生成硝酸亚铁.
B.向NaHCO3溶液中加入过量的澄清石灰水,反应生成碳酸钙、氢氧化钠和水;
C.二氧化碳过量,反应生成碳酸氢根离子;
D.16.8g 铁粉物质的量=
| 16.8g |
| 56g/mol |
解答:
解:A.HCO3-的水解方程式可表示为:HCO3-+H2O?HO-+H2CO3,故A错误;
B.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀,离子方程式:HCO3-+Ca2++OH-═CaCO3↓+H2O,故C错误;
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故C错误;
D.将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)铁粉过量,反应生成硝酸亚铁,离子方程式:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故D正确;
故选:D.
B.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀,离子方程式:HCO3-+Ca2++OH-═CaCO3↓+H2O,故C错误;
C.向NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故C错误;
D.将16.8g 铁粉投入100mL 4.0mol/L的HNO3溶液中(还原产物只有NO)铁粉过量,反应生成硝酸亚铁,离子方程式:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故D正确;
故选:D.
点评:本题考查了离子方程式的书写,题目难度不大,明确反应的实质是解题关键,注意反应物用量对反应的影响,选项BD为易错选项.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
常温下,水的电离达到平衡:H2O?H++OH-△H>0.下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+) 降低 |
| D、将水加热,KW增大,pH不变 |
100mLpH=11的氨水与100mLpH=3的盐酸相混合,所得的混合液( )
| A、显碱性 | B、显酸性 |
| C、显中性 | D、不能确定其酸碱性 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、0.1mol/L NH4+ 中含有质子数为NA |
| B、26g 乙炔中含有π键数为2NA |
| C、标准状况下,22.4L SO3 中所含分子数为NA |
| D、1L 0.1mol/L NaHCO3 溶液中所含氧原子数为0.3NA |
下列反应的离子方程式正确的是( )
| A、氯化铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO2-+4NH4++2H2O | ||||
B、NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-
| ||||
| C、漂白粉溶液中通入足量的SO2气体:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | ||||
| D、明矾溶液与氢氧化钡溶液反应,使 SO2-恰好完全沉淀:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表下列判断不正确的是( )
| 实验编号 | c(HA)/mol?L-1 | c(NaOH)/mol?L-1 | 混合溶液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.2 | 0.2 | pH=9 |
| 丙 | c1 | 0.2 | pH=7 |
| 丁 | 0.2 | 0.1 | pH<7 |
| A、a<9 |
| B、c1<0.2 |
| C、在乙组混合溶液中c(OH-)-c(HA)=10-9 mol/L |
| D、在丁组混合液中c(Na+)<c(A-) |
向FeI2溶液中滴加适量氯水,将反应后溶液分3份,甲试管中滴加淀粉溶液,乙试管滴加KSCN溶液,丙试管中滴加酸性高锰酸钾溶液,下列说法正确的是( )
| A、若甲试管溶液呈蓝色,则乙试管溶液一定呈血红色 |
| B、若甲试管溶液呈蓝色,则乙试管溶液可能无明显现象 |
| C、乙试管溶液呈血红色,则甲试管溶液不可能呈蓝色 |
| D、甲试管溶液呈蓝色,丙试管中紫红色褪去,说明滴加氯水后的溶液中一定存在Fe3+和Fe2+ |
下列各组离子能大量共存的是( )
| A、Ag+ NO3- Cl- H+ |
| B、Ba2+ SO42- NO3- Na+ |
| C、Ba2+ Mg2+ NO3- Cl- |
| D、CO32- H+ OH- Ca2+ |
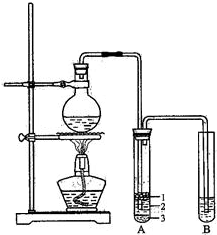 根据题意完成下列填空:有关数据列表如下:
根据题意完成下列填空:有关数据列表如下: