题目内容
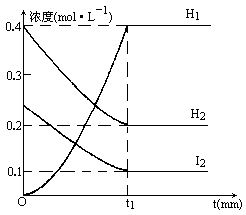
可逆反应:H2(g)+I2(g)![]() 2HI(g),在一定条件下,反应物和生成物的浓度随时间的变化曲线如下图回答:①t1表示________;②当时间由0到t1 min的间隔里,H2的平均反应速率是________;③氢气的转化率是________;④升高温度后氢气的转化率为40%,则合成HI的反应是________热反应.
2HI(g),在一定条件下,反应物和生成物的浓度随时间的变化曲线如下图回答:①t1表示________;②当时间由0到t1 min的间隔里,H2的平均反应速率是________;③氢气的转化率是________;④升高温度后氢气的转化率为40%,则合成HI的反应是________热反应.
解析:
|
①达到平衡的时间 ② ③50% ④放 |

 导学教程高中新课标系列答案
导学教程高中新课标系列答案相同温度下,在四个密闭容器中发生可逆反应:H2(g)+I2(g)![]() 2HI(g),实验测得起始、平衡时的有关数据如下表所示:
2HI(g),实验测得起始、平衡时的有关数据如下表所示:
| 容器编号 | 起始时各物质的物质的量(mol) | 达平衡时体系的变化 | ||
| I2 | H2 | HI | ||
| ① | 1 | 3 | 0 | 放出热量:Q1=23.15kJ |
| ② | 0.8 | 2.8 | 0.4 | 平衡时碘化氢的体积分数为20% |
| ③ | 0 | 4 | 4 |
|
| ④ | 2 | 3 | 0 |
|
(1)下列叙述正确的是
A.四个容器中反应的平衡常数相等
B.反应的热化学方程式为:H2(g)+I2(g)![]() 2HI(g) △ H =23.15kJ/mol
2HI(g) △ H =23.15kJ/mol
C.平衡时,容器④中H2的转化率高于① D、容器②中达平衡时放出的热量Q2<23.15kJ
E、达到平衡后若将容器①的体积变为0.25 L,H2的转化率提高
(2)该温度下,在容积为1L密闭容器③中发生反应建立平衡,若达到平衡所需的时间为2min,则平均反应速率v(HI)= ,该温度下,反应H2(g)+I2(g)![]() 2HI(g)的平衡常数 K= 。
2HI(g)的平衡常数 K= 。
(3)平衡常数K只受温度的影响,与浓度、压强等因素无关,故可利用平衡常数来判断平衡是否移动及移动的方向。例如,若③为一个装有可移动活塞的容器,上述平衡达成后用外力将活塞向内推至容积为0.5L并恢复原温度,则由于
 ,
,
可判断平衡将 (填“正向”、“逆向”或“不”)移动。
(4)如果保持温度和压强不变,向③的平衡体系中加入1.6molI2,平衡将 (填“正向”、“逆向”或“不”)移动,理由是 。
密闭容器中发生可逆反应:H2(g)+I2(g)  2HI(g) 达到平衡状态时的标志是
2HI(g) 达到平衡状态时的标志是
| A.容器的压强恒定不变 |
| B.混合气体的颜色不再改变 |
| C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
相同温度下,在四个密闭容器中发生可逆反应:H2(g)+I2(g) 2HI(g),实验测得起始、平衡时的有关数据如下表所示:
2HI(g),实验测得起始、平衡时的有关数据如下表所示:
|
容器编号[来源:学_科_网] |
起始时各物质的物质的量(mol)[来源:ZXXK][来源:学_科_网Z_X_X_K][来源:学|科|网] |
达平衡时体系的变化[来源:学+科+网Z+X+X+K] |
||
|
I2 |
H2 |
HI |
||
|
① |
1 |
3 |
0 |
放出热量:Q1=23.15kJ |
|
② |
0.8 |
2.8 |
0.4 |
平衡时碘化氢的体积分数为20% |
|
③ |
0 |
4 |
4 |
|
|
④ |
2 |
3 |
0 |
|
(1)下列叙述正确的是
A.四个容器中反应的平衡常数相等
B.反应的热化学方程式为:H2(g)+I2(g) 2HI(g) △ H =23.15kJ/mol
2HI(g) △ H =23.15kJ/mol
C.平衡时,容器④中H2的转化率高于① D、容器②中达平衡时放出的热量Q2<23.15kJ
E、达到平衡后若将容器①的体积变为0.25 L,H2的转化率提高
(2)该温度下,在容积为1L密闭容器③中发生反应建立平衡,若达到平衡所需的时间为2min,则平均反应速率v(HI)= ,该温度下,反应H2(g)+I2(g) 2HI(g)的平衡常数 K=
。
2HI(g)的平衡常数 K=
。
(3)平衡常数K只受温度的影响,与浓度、压强等因素无关,故可利用平衡常数来判断平衡是否移动及移动的方向。例如,若③为一个装有可移动活塞的容器,上述平衡达成后用外力将活塞向内推至容积为0.5L并恢复原温度,则由于
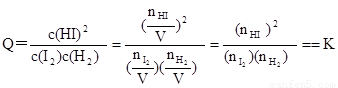 ,
,
可判断平衡将 (填“正向”、“逆向”或“不”)移动。
(4)如果保持温度和压强不变,向③的平衡体系中加入1.6molI2,平衡将 (填“正向”、“逆向”或“不”)移动,理由是 。
 2HI
(g)达到平衡的标志是
2HI
(g)达到平衡的标志是 2HI(g),在温度一定下,从正方向开始发生反应,下列说法正确的是
2HI(g),在温度一定下,从正方向开始发生反应,下列说法正确的是