题目内容
在一固定容积的密闭容器中,可逆反应: H2(g) + I2(g) 2HI
(g)达到平衡的标志是
2HI
(g)达到平衡的标志是
A.H2、I2、HI的分子数之比为1∶1∶2
B.混合气体的颜色不再发生变化
C.单位时间生成n mol H2,同时消耗成2n mol HI
D.混合气体的密度保持不变
B
【解析】
试题分析:A.反应H2(g) + I2(g) 2HI
(g)是一个反应前后气体体积相等的反应。当H2、I2、HI的分子数之比为1∶1∶2时反应可能达到平衡,也可能未达到平衡故不能作为平衡的标志。错误。B.在H2、I2、HI三种分子中只有I2是有颜色的。由于容器的容积固定不变,所以当混合气体的颜色不再发生变化,说明C(I2)不变,n(I2).反应就达到了平衡状态。正确。C.在任何时刻,单位时间每生成n mol H2,必同时消耗成2n mol
HI,这时反应逆向进行的二者关系。所以不能作为判断平衡状态的标志。错误。D.容器的容积不变,无论是否反应混合气体的质量不变,所以密度也就保持不变。所以不能作为判断平衡状态的标志。错误。
2HI
(g)是一个反应前后气体体积相等的反应。当H2、I2、HI的分子数之比为1∶1∶2时反应可能达到平衡,也可能未达到平衡故不能作为平衡的标志。错误。B.在H2、I2、HI三种分子中只有I2是有颜色的。由于容器的容积固定不变,所以当混合气体的颜色不再发生变化,说明C(I2)不变,n(I2).反应就达到了平衡状态。正确。C.在任何时刻,单位时间每生成n mol H2,必同时消耗成2n mol
HI,这时反应逆向进行的二者关系。所以不能作为判断平衡状态的标志。错误。D.容器的容积不变,无论是否反应混合气体的质量不变,所以密度也就保持不变。所以不能作为判断平衡状态的标志。错误。
考点:考查化学平衡状态的判断的标志问题。

氮是大气中含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用,减少氮氧化物的排放是环境保护的重要内容之一。请回答下列氮及其化合物的相关问题:
(1)据报道,意大利科学家获得了极具研究价值的N4,其分子结构与白磷分子的正四面体结构相似。已知断裂1 mol N-N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量,请写出N4气体转变为N2反应的热化学方程式: 。
(2)据报道,NH3可直接用作车用燃料电池,写出该电池的负极反应式: 。
(3)在T1℃时,将5 mol N2O5置于10L固定容积的密闭容器中发生下列反应:2N2O5(g) 4NO2(g)+O2(g);△H>0。反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。
4NO2(g)+O2(g);△H>0。反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。
①求该反应的平衡常数K= (数字代入式子即可),上述平衡体系中O2的体积分数为__________。
②用O2表示从0~5 min内该反应的平均速率υ(O2)= 。
③将上述平衡体系的温度降至T2℃,密闭容器内减小的物理量有 。
A.压强 B.密度 C.反应速率 D.N2O5的浓度
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g) N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是__________。
N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是__________。
A.都引起a减小 B.都引起a增大 C.充入NO2引起a减小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a减小
 氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.
氮是地球上含量丰富的元素,氮及其化合物的研究在生产、生活中有着重要意义.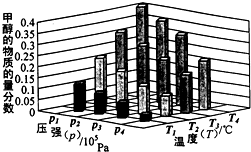 能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
能源是制约国家发展进程的因素之一.甲醇、二甲醚等被称为2 1世纪的绿色能源,工业上利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚. 4NO2(g)+O2(g);△H>0。反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。
4NO2(g)+O2(g);△H>0。反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%。