题目内容
6.2.5 mol C(石墨)在O2中完全燃烧生成CO2,放出多少热量?分析 101kPa时,1mol C(石墨)完全燃烧放出393.5kJ的热量,物质燃烧放出的热量与物质的物质的量成正比.
解答 解:1mol C(石墨)完全燃烧放出393.5kJ的热量,2.5mol C(石墨)在O2中完全燃烧生成CO2,放出的热量:2.5mol×393.5kJ/mol=983.75kJ,
答:2.5mol C(石墨)在O2中完全燃烧生成CO2,放出983.75kJ热量.
点评 本题以化学方程式有关计算为载体考查燃烧热的有关计算,为高频考点,明确放出热量与物质的量关系是解本题关键,题目难度不大.

练习册系列答案
相关题目
16.根据键能数据估算CH4(g)+4F2(g)═CF4+4HF(g)的反应热△H为( )
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/(kJ/mol) | 414 | 489 | 565 | 155 |
| A. | -485kj/mol | B. | +485kj/mol | C. | +l940kj/mol | D. | -l940kj/mol |
17.下列关于Na2CO3的说法中正确的是( )
| A. | Na2CO3溶液中c(OH-)=c(H+)+c(HCO3-)+c(H2CO3) | |
| B. | Na2CO3溶液中滴加酚酞呈红色,加热红色变浅 | |
| C. | 0.1mol•L-1的Na2CO3溶液中c(Na+)>2c(CO32-) | |
| D. | 相同温度下,CaCO3在饱和Na2CO3溶液中的KSP比在纯水中的小 |
1.下列按照由大到小排列正确的是( )
| A. | 密度:Cs Rb K Na Li | B. | 溶解度:NaHC03 Na2C03 CaC03 | ||
| C. | 氧化性:Li+Na+K+ Rb+Cs+ | D. | 碱性:LiOH NaOH KOH RbOH CsOH |
11.下列说法正确的是( )
| A. | 自发进行的反应一定时放热反应 | B. | 非自发进行的反应一定是吸热反应 | ||
| C. | 自发进行的反应一定能发生 | D. | 有些吸热反应也能自发进行 |
3.N2O5是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 .
.
(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
则500s内N2O5的分解速率为0.00296 mol•L-1•s-1.
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.
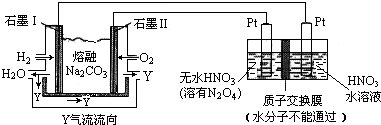
写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
 .
.(2)一定温度下,在恒容密闭容器中N2O5可发生下列反应:2N2O5(g)?4NO2(g)+O2(g);△H>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将不变(填“增大”、“减小”、“不变”).
②如表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol•L-1 | 5.00 | 3.52 | 2.48 |
③在T2温度下,反应1000s时测得NO2的浓度为4.98mol•L-1,则T2<T1(填>、<或=).
(3)现以H2、O2、熔融Na2CO3组成的燃料电池采用电解法制备N2O5,装置如图所示,其中Y为CO2.

写出石墨Ⅰ电极上发生反应的电极反应式H2+CO32--2e-═H2O+CO2,N2O5在电解池的阳极区生成(填“阳极”或“阴极”).