题目内容
【题目】下列各组离子在指定溶液中,能大量共存的是( )
![]() 无色溶液中:
无色溶液中:![]()
![]()
![]()
![]()
![]()
![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 水电离的
水电离的![]() 浓度为
浓度为![]() 的溶液中:
的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 加入铝粉放出氢气的溶液中:
加入铝粉放出氢气的溶液中:![]()
![]()
![]()
![]()
![]()
![]()
![]() 使甲基橙变红的溶液中:
使甲基橙变红的溶液中:![]()
![]()
![]()
![]()
![]()
![]() 中性溶液中:
中性溶液中:![]()
![]()
![]()
![]()
![]() 能溶解铜粉的溶液:
能溶解铜粉的溶液:![]()
![]()
![]()
![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
【答案】D
【解析】
![]() 为橙色,与无色不符,故不符合题意;
为橙色,与无色不符,故不符合题意;
![]() 的溶液显碱性,该组离子之间不反应,可大量共存,故符合题意;
的溶液显碱性,该组离子之间不反应,可大量共存,故符合题意;
![]() 常温下水电离的
常温下水电离的![]() 浓度为
浓度为![]() 的溶液,水的电离被促进,溶液显酸性或碱性,酸性溶液中不能大量存在
的溶液,水的电离被促进,溶液显酸性或碱性,酸性溶液中不能大量存在![]() 、
、![]() ,碱性溶液中不能大量存在铵根离子,故不符合题意;
,碱性溶液中不能大量存在铵根离子,故不符合题意;
![]() 加入铝粉放出氢气的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在
加入铝粉放出氢气的溶液,为非氧化性酸或强碱溶液,碱性溶液中不能存在![]() 、
、![]() ,酸性溶液中
,酸性溶液中![]() 不能大量存在,故不符合题意;
不能大量存在,故不符合题意;
![]() 使甲基橙变红的溶液显酸性,MnO4-、NO3-(H+)与Fe2+发生氧化还原反应,不能大量共存,故不符合题意;
使甲基橙变红的溶液显酸性,MnO4-、NO3-(H+)与Fe2+发生氧化还原反应,不能大量共存,故不符合题意;
![]() 中性溶液不能大量存在
中性溶液不能大量存在![]() 、
、![]() ,故不符合题意;
,故不符合题意;
![]() 能溶解铜粉的溶液,具有氧化性物质,不能存在还原性离子
能溶解铜粉的溶液,具有氧化性物质,不能存在还原性离子![]() ,且
,且![]() 、
、![]() 发生氧化还原反应,不能大量共存,故不符合题意;
发生氧化还原反应,不能大量共存,故不符合题意;
综上能大量共存的只有②;
故选D。

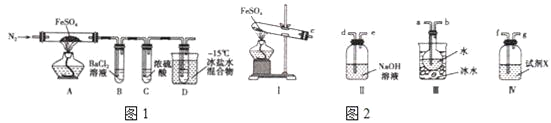
【题目】某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气。
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子。
Ⅲ.接着再向B中通入一定量的SO2气体。
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子。
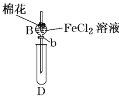
(1)棉花中浸润的溶液为____________,目的是____________________
(2)过程Ⅲ中一定发生反应的离子方程式为________________________________,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是______________________________________。
(3)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是___________________________。
(4)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是______________。
过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
甲 | 有Fe3+无Fe2+ | 有SO42- |
乙 | 既有Fe3+又有Fe2+ | 有SO42- |
丙 | 有Fe3+无Fe2+ | 有Fe2+ |