题目内容
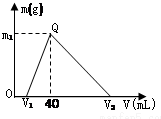 常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )
常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到200mL c(OH-)=0.1mol/L的溶液,然后逐滴加入1mol/L的盐酸,测得生成沉淀的质量m与消耗盐酸的体积V关系如图所示,则下列说法正确的是( )| A、原合金质量为 0.92 g |
| B、图中V2为 100 |
| C、整个加入盐酸过程中 Na+的浓度保持不变 |
| D、Q点m1为0.78 |
考点:离子方程式的有关计算
专题:
分析:钠铝合金置于水中,合金全部溶解,发生2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,加盐酸时发生NaOH+HCl═NaCl+H2O、NaAlO2+HCl+H2O═NaCl+Al(OH)3↓、Al(OH)3↓+3HCl═AlCl3+3H2O,再结合图象中加入40mL盐酸生成的沉淀最多来计算.
解答:
解:由图象可知,向合金溶解后的溶液中加盐酸,先发生NaOH+HCl═NaCl+H2O,后发生NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,最后发生Al(OH)3↓+3HCl═AlCl3+3H2O,
合金溶解后剩余的氢氧化钠的物质的量为0.2L×0.1mol/L=0.02mol,由NaOH+HCl═NaCl+H2O,则V1为
=0.02L=20mL,生成沉淀时消耗的盐酸为40mL-20mL=20mL,其物质的量为0.02L×1mol/L=0.02mol,
由 NaAlO2 +HCl+H2O═NaCl+Al(OH)3↓,
0.02mol 0.02mol 0.02mol
A、由钠元素及铝元素守恒可知,合金的质量为0.04mol×23g/mol+0.02mol×27g/mol=1.46g,故A错误;
B、由Al(OH)3↓+3HCl═AlCl3+3H2O可知,溶解沉淀需要0.06molHCl,其体积为60mL,则V2为40mL+60mL=100mL,故B正确;
C、由2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,加盐酸后,先发生NaOH+HCl═NaCl+H2O,后发生NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,最后发生Al(OH)3↓+3HCl═AlCl3+3H2O,随着盐酸的量的加入,体积增大,钠离子的量不变,所以浓度减小,故C错误;
D、由上述计算可知,生成沉淀为0.02mol,其质量为0.02mol×78g/mol=1.56g,故D错误;
故选B.
合金溶解后剩余的氢氧化钠的物质的量为0.2L×0.1mol/L=0.02mol,由NaOH+HCl═NaCl+H2O,则V1为
| 0.02mol |
| 1mol/L |
由 NaAlO2 +HCl+H2O═NaCl+Al(OH)3↓,
0.02mol 0.02mol 0.02mol
A、由钠元素及铝元素守恒可知,合金的质量为0.04mol×23g/mol+0.02mol×27g/mol=1.46g,故A错误;
B、由Al(OH)3↓+3HCl═AlCl3+3H2O可知,溶解沉淀需要0.06molHCl,其体积为60mL,则V2为40mL+60mL=100mL,故B正确;
C、由2Na+2H2O═2NaOH+H2↑、2Al+2H2O+2NaOH═2NaAlO2+3H2↑,加盐酸后,先发生NaOH+HCl═NaCl+H2O,后发生NaAlO2+HCl+H2O═NaCl+Al(OH)3↓,最后发生Al(OH)3↓+3HCl═AlCl3+3H2O,随着盐酸的量的加入,体积增大,钠离子的量不变,所以浓度减小,故C错误;
D、由上述计算可知,生成沉淀为0.02mol,其质量为0.02mol×78g/mol=1.56g,故D错误;
故选B.
点评:本题考查钠、铝的化学性质及反应,明确发生的化学反应及反应与图象的对应关系是解答本题的关键,并学会利用元素守恒的方法来解答,难度较大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、BaSO4不溶于水,其水溶液很难导电,所以BaSO4是非电解质 |
| C、液氯不导电,所以液氯是非电解质 |
| D、氯化氢的水溶液能导电,所以氯化氢是电解质 |
用NA表示阿伏伽德罗常数,下列说法不正确的是( )
| A、2mol SO2和1mol O2在一定条件下反应,反应后分子总数大于2NA |
| B、25℃,在pH=2的1.0L H2SO4溶液中含有H+数目为0.01NA |
| C、在二氧化硅的晶体中,1mol SiO2含有Si-O键数目为NA |
| D、25mL 18mol?L-1浓硫酸与足量Zn反应,转移电子数为0.225NA |
有一可逆反应2A(g)+3B(g)?4C(g)+D(g),已知起始浓度c(A)=2mol/L,c(B)=3mol/L,c(C)=c(D)=0,反应开始20min后达到平衡状态,此时D的平衡浓度为0.5mol/L,则下列说法不正确的是( )
| A、前20 min的平均反应速率v(C)=0.1 mol/(L?min) |
| B、A的转化率为50% |
| C、C的平衡浓度c(C)=4 mol/L |
| D、B的平衡浓度c(B)=1.5 mol/L |
下列说法正确的是( )
| A、物质的量浓度和体积都相同的盐酸和醋酸溶液,在与足量锌反应时,起始时二者产生H2速率基本相等 |
| B、100 mL 1 mol?L-1的盐酸和50 mL 2 mol?L-1的盐酸,分别与足量的锌反应时,两者放出H2速率和质量均相等 |
| C、100 mL pH=3的H2SO4和HCl溶液,与足量锌反应后,放出H2的质量相等 |
| D、100 mL pH=3的盐酸与醋酸溶液,与足量锌反应后,所得H2的质量相等 |
 +R
+R +R
+R