题目内容
已知X、Y、Z、W四种元素分别是连续三个短周期的元素,且原子序数依次增大.X、W同主族,Y、Z为同周期的相邻元素.W原子的质子数等于Y、Z原子最外层电子数之和.Y与X形成的分子中有3个共价键.Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)X,Z两种元素的元素符号:X 、Z .
(2)由以上元素中两两形成的化合物中:
溶于水显碱性的气态氢化物的电子式为 ;它的共价键属于 (填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为 ;含有极性共价键和非极性共价键的化合物的电子式为 .
(3)由X、Y、Z所形成的常见离子化合物是 (写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为: ;X与W形成的化合物与水反应时,水是 (填“氧化剂”或“还原剂”).
(4)用电子式表示W与Z形成W2Z的过程: .
(1)X,Z两种元素的元素符号:X
(2)由以上元素中两两形成的化合物中:
溶于水显碱性的气态氢化物的电子式为
(3)由X、Y、Z所形成的常见离子化合物是
(4)用电子式表示W与Z形成W2Z的过程:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以Z元素是O元素;Y、Z为同周期的相邻元素,Y与X形成的分子中有3个共价键,X的原子序数最小且能和Y形成共价键,则X和Y都是非金属元素,Y的原子序数小于8,所以Y是N元素,X是H元素;X、W同主族,W原子的质子数等于Y、Z原子最外层电子数之和,则W是Na元素,据此答题;
解答:
解:X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以Z元素是O元素;Y、Z为同周期的相邻元素,Y与X形成的分子中有3个共价键,X的原子序数最小且能和Y形成共价键,则X和Y都是非金属元素,Y的原子序数小于8,所以Y是N元素,X是H元素;X、W同主族,W原子的质子数等于Y、Z原子最外层电子数之和,则W是Na元素,
(1)根据上面的分析可知,X为H元素,Z为O元素,
故答案为:H;O;
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物为氨气,它的电子式为 ;它的共价键属于极性键;含有离子键和非极性共价键的化合物为过氧化钠,它的电子式为
;它的共价键属于极性键;含有离子键和非极性共价键的化合物为过氧化钠,它的电子式为 ;含有极性共价键和非极性共价键的化合物为双氧水或肼,它们的电子式为
;含有极性共价键和非极性共价键的化合物为双氧水或肼,它们的电子式为 或
或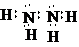 ,
,
故答案为: ;极性;
;极性; ;
; 或
或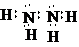 ;
;
(3)由X、Y、Z所形成的常见离子化合物是NH4NO3,该化合物与氢氧化钠的浓溶液加热时反应的离子方程式为:NH4++OH-
NH3↑+H2O;X与W形成的化合物为氢化钠,与水反应时水是氧化剂,
故答案为:NH4NO3;NH4NO3;NH4++OH-
NH3↑+H2O;氧化剂;
(4)W2Z为氧化钠,用电子式表示氧化钠的形成过程为 ,
,
故答案为: ;
;
(1)根据上面的分析可知,X为H元素,Z为O元素,
故答案为:H;O;
(2)由以上元素中两两形成的化合物中:溶于水显碱性的气态氢化物为氨气,它的电子式为
 ;它的共价键属于极性键;含有离子键和非极性共价键的化合物为过氧化钠,它的电子式为
;它的共价键属于极性键;含有离子键和非极性共价键的化合物为过氧化钠,它的电子式为 ;含有极性共价键和非极性共价键的化合物为双氧水或肼,它们的电子式为
;含有极性共价键和非极性共价键的化合物为双氧水或肼,它们的电子式为 或
或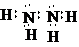 ,
,故答案为:
 ;极性;
;极性; ;
; 或
或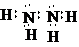 ;
;(3)由X、Y、Z所形成的常见离子化合物是NH4NO3,该化合物与氢氧化钠的浓溶液加热时反应的离子方程式为:NH4++OH-
| ||
故答案为:NH4NO3;NH4NO3;NH4++OH-
| ||
(4)W2Z为氧化钠,用电子式表示氧化钠的形成过程为
 ,
,故答案为:
 ;
;
点评:本题主要考查了电子式、离子反应方程式、化学键等知识点,中等难度,解题关键在于元素推断,答题时注意化学用语的规范表达.

练习册系列答案
相关题目
下列化学用语表示正确的是( )
A、甲基的电子式: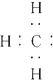 |
B、氮原子的电子排布图: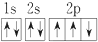 |
| C、氯离子的最外层电子排布:3s23p6 |
D、硫原子的结构示意图: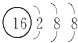 |
下列表示对应化学反应的离子方程式正确的是( )
| A、铜溶于FeCl3溶液:Cu+Fe3+=Cu2++Fe2+ |
| B、Na[Al(OH)4]溶液中通入过量CO2:[Al(OH)4]-+CO2=Al(OH)3↓+CO32- |
| C、氯化铝溶液中加过量氨水:Al3++3OH-═Al(OH)3↓ |
| D、次氯酸钠溶液中滴入浓盐酸产生氯气:ClO-+Cl-+2H+=Cl2↑+H2O |
下列有关叙述正确的是( )
| A、元素原子最外层电子数的多少是判断金属性和非金属性强弱的依据 |
| B、OH-与H3O+组成元素相同,所含质子数相同 |
C、结构示意图为 和 和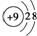 两种粒子为同一种元素 两种粒子为同一种元素 |
| D、H、D、T具有相同的质子数,是氢元素的三种同位素 |
对于可逆反应:A(g)+2B(g)?nC(g),符合如图关系的结论是( )


| A、P1>P2,n<3 |
| B、P1>P2,n>3 |
| C、P1<P2,n>3 |
| D、P1<P2,n<3 |
已知1-18号元素的离子aW3+、bX+、CY2-、dZ-都具有相同的电子层结构,则下列叙述或表示方法正确的是( )
| A、四种元素位于同一周期 |
| B、氢化物的稳定性H2Y>HZ |
| C、离子的氧化性aW3+>bX+ |
| D、原子半径Z>Y |
 有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中M(C3H4O)和A均能发生银镜反应.N和M的分子中碳原子数相同,A的烃基上的一氯取代位置有三种.
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程生产的.图中M(C3H4O)和A均能发生银镜反应.N和M的分子中碳原子数相同,A的烃基上的一氯取代位置有三种.