题目内容
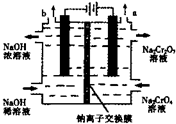 某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )
某工厂采用石墨电极电解Na2CrO4溶液,实现Na2CrO4到 Na2Cr2O7的转化,其装置如图所示.下列说法正确的是( )分析:A、通过电解提高阳极区溶液的酸性,实现Na2CrO4转化为Na2Cr2O7;
B、电解池中钠离子从阳极移向阴极;
C、电解池中阴极被保护不参与反应;
D、通过电解提高阳极区溶液的酸性,说明在阳极区生成H+,电极反应式为2H2O-4e-=O2+4H+,2CrO42-+2H+=Cr2O72-+H2O.
B、电解池中钠离子从阳极移向阴极;
C、电解池中阴极被保护不参与反应;
D、通过电解提高阳极区溶液的酸性,说明在阳极区生成H+,电极反应式为2H2O-4e-=O2+4H+,2CrO42-+2H+=Cr2O72-+H2O.
解答:解:A、通过电解提高阳极区溶液的酸性,说明在阳极区生成H+,电极反应式为2H2O-4e-=O2+4H+,2CrO42-+2H+=Cr2O72-+H2O;溶液PH不会不断下降,故A错误;
B、电解池中阳离子移向阴极,钠离子从阳极移向阴极,故B错误;
C、电解池中阴极被保护不参与反应,可以用铁做阴极,故C错误;
D、通过电解提高阳极区溶液的酸性,说明在阳极区生成H+,电极反应式为2H2O-4e-=O2+4H+,2CrO42-+2H+=Cr2O72-+H2O,故D正确;
故选D.
B、电解池中阳离子移向阴极,钠离子从阳极移向阴极,故B错误;
C、电解池中阴极被保护不参与反应,可以用铁做阴极,故C错误;
D、通过电解提高阳极区溶液的酸性,说明在阳极区生成H+,电极反应式为2H2O-4e-=O2+4H+,2CrO42-+2H+=Cr2O72-+H2O,故D正确;
故选D.
点评:本题考查了电解池原理的分析应用,电极判断,电极反应是解题关键,题目难中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目


 ),聚丙烯酸钠单体的结构简式是________;
),聚丙烯酸钠单体的结构简式是________;