题目内容
14.给定条件下,下列选项中所示的物质间转化均能一步实现的是( )| A. | S$→_{点燃}^{O_{2}}$SO2$\stackrel{BaCl_{2}(aq)}{→}$BaSO4 | |
| B. | SiO2$\stackrel{H_{2}O}{→}$H2SiO3$\stackrel{NaOH(aq)}{→}$Na2SiO3(aq) | |
| C. | MgCl2•6H2O $\stackrel{△}{→}$MgCl2$\stackrel{通电}{→}$Mg | |
| D. | CuSO4(aq)$\stackrel{NaOH(aq)}{→}$Cu(OH)2悬浊液$→_{△}^{葡萄糖}$Cu2O |
分析 A、二氧化硫与氯化钡不反应;
B、二氧化硅不溶于水;
C、MgCl2•6H2O要在氯化氢的氛围中加热得到氯化镁固体;
D、硫酸铜和氢氧化钠反应生成氢氧化铜,氢氧化铜和葡萄糖加热反应生成氧化亚铜红色沉淀.
解答 解:A、二氧化硫与氯化钡不反应,弱酸不能制强酸,故A错误;
B、二氧化硅不溶于水,二氧化硅与水不反应,故B错误;
C、MgCl2•6H2O要在氯化氢的氛围中加热得到氯化镁固体,故C错误;
D、硫酸铜和氢氧化钠反应生成氢氧化铜,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4,氢氧化铜和葡萄糖加热反应生成氧化亚铜红色沉淀,C6H12O6+2Cu(OH)2$\stackrel{△}{→}$CH2(OH)(CHOH)4COOH+Cu2O↓+2H2O,所以能实现转化,故D正确;
故选D.
点评 本题考查了物质性质转化关系的分析判断,主要是我在性质和反应条件的分析应用,掌握元素化合物性质和反应实质是关键,题目难度中等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
16.现有浓度为0.02mol/L的HCN与0.01mol/LNaOH等体积混合后,测得c(Na+)>c(CN-),下列关系正确的是( )
| A. | c(H+)>c(OH-) | B. | c(H+)<c(OH-) | ||
| C. | c(H+)+c(HCN)=c(OH-) | D. | c(HCN)+c(CN-)=0.01mol/L |
5.下列化合物中含有共价键的是( )
| A. | HCl | B. | Na2O | C. | KBr | D. | MgCl2 |
9.用NA表示阿佛加德罗常数的值,下列各项说法中正确的是( )
| A. | 一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA | |
| B. | 一定条件下用含1mol FeCl3的溶液制备Fe(OH)3胶体,产生NA个Fe(OH)3胶粒 | |
| C. | 标准状况下,22.4L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
19.下列叙述正确的是( )
| A. | 标准状况下,1molCCl4的体积约为22.4L | |
| B. | 0℃、101KPa时,2g氢气的体积约为22.4L | |
| C. | 通常状况下,22.4LCO2中所含分子数为NA个 | |
| D. | 1mol气体的体积只有在标准状况下才约为22.4L |
6.下列对乙烯和聚乙烯的描述中,不正确的是( )
| A. | 乙烯是纯净物,聚乙烯是混合物 | |
| B. | 常温下,乙烯为气态,聚乙烯为固态 | |
| C. | 乙烯的化学性质与聚乙烯相同 | |
| D. | 取等质量的乙烯和聚乙烯完全燃烧后,生成的CO2和H2O的质量分别相等 |
3.如图所示,下列实验现象预测或操作正确的是( )
| A. | 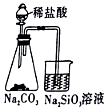 如图,可以证明非金属性强弱:Cl>C>Si | |
| B. | 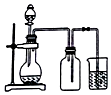 如图,用铜片和稀硝酸制NO | |
| C. | 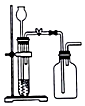 如图,用锌粒和稀硫酸制H2 | |
| D. | 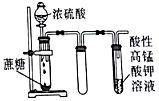 如图,酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去 |
9.用下列实验装置进行相应实验,能达到实验目的是( )


| A. | 用装置甲制取氨气 | B. | 用装置乙制取少量纯净的CO2气体 | ||
| C. | 用装置丙验证氨气具有还原性 | D. | 用装置丁吸收尾气氨气 |