题目内容
(1)标准状况下 ①6.72L甲烷(CH4) ②3.01x1023个HCl分子 ③13.6gH2S 三种气体中所含氢原子数从小到大的排列 .(用序号填写)
(2)0.3mol NH3 分子中所含质子数与 个H2O分子中所含质子数相等.
(3)含0.4mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是 .
(4)已知16g A和20g B 恰好完全反应生成0.04mol C 和31.76g D,则C的摩尔质量为 .
(2)0.3mol NH3 分子中所含质子数与
(3)含0.4mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是
(4)已知16g A和20g B 恰好完全反应生成0.04mol C 和31.76g D,则C的摩尔质量为
考点:物质分子中的原子个数计算,物质的量的相关计算
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)先根据n=
计算6.72LCH4的物质的量,根据n=
计算HCl的物质的量,根据n=
计算13.6gH2S的物质的量,再根据各分子含有的H原子数目,计算各物质含有的H原子物质的量,据此判断;
(2)根据物质的物质的量以及1个分子中含有的质子数来计算;
(3)根据Al2(SO4)3中n(Al3+):n(SO42-)=2:3计算n(SO42-);
(4)先根据质量守恒计算C的质量,再根据M=
计算其摩尔质量.
| V |
| Vm |
| N |
| NA |
| m |
| M |
(2)根据物质的物质的量以及1个分子中含有的质子数来计算;
(3)根据Al2(SO4)3中n(Al3+):n(SO42-)=2:3计算n(SO42-);
(4)先根据质量守恒计算C的质量,再根据M=
| m |
| n |
解答:
解:(1)6.72LCH4的物质的量为
=0.3mol,3.01×1023个HCl的物质的量为
=0.5mol,13.6gH2S的物质的量为
=0.4mol,CH4中n(H)=0.3mol×4=1.2mol,HCl中n(H)=0.5mol,硫化氢中n(H)=0.4mol×2=0.8mol,氨气中n(H)=0.2mol×3=0.6mol,故H原子数目②<③<①,
故答案为:②<③<①;
(2)1个NH3分子中含有10个质子,1个H2O分子中含有10个质子,0.3molNH3分子中所含质子数为3mol,所以H2O的物质的量为0.3mol,数目为0.3×6.02×1023=1.806×1023,
故答案为:1.806×1023;
(3)Al2(SO4)3中n(Al3+):n(SO42-)=2:3,n(Al3+)=0.4mol,则n(SO42-)=0.6mol,
故答案为:0.6mol;
(4)16克A和20克B恰好完全反应生成0.04摩尔C和31.76g D,根据质量守恒知,C的质量为4.24g,M=
=
=106g/mol,
故答案为:106g/mol.
| 6.72L |
| 22.4L/mol |
| 3.01×1023 |
| 6.02×1023mol-1 |
| 13.6g |
| 34g/mol |
故答案为:②<③<①;
(2)1个NH3分子中含有10个质子,1个H2O分子中含有10个质子,0.3molNH3分子中所含质子数为3mol,所以H2O的物质的量为0.3mol,数目为0.3×6.02×1023=1.806×1023,
故答案为:1.806×1023;
(3)Al2(SO4)3中n(Al3+):n(SO42-)=2:3,n(Al3+)=0.4mol,则n(SO42-)=0.6mol,
故答案为:0.6mol;
(4)16克A和20克B恰好完全反应生成0.04摩尔C和31.76g D,根据质量守恒知,C的质量为4.24g,M=
| m |
| n |
| 4.24g |
| 0.04mol |
故答案为:106g/mol.
点评:本题考查物质的量的相关计算,侧重于学生的分析能力和计算能力的考查,难度不大,注意相关计算公式的运用

练习册系列答案
相关题目
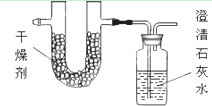 某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).
某烃CxHy同温同压条件下测得其蒸汽的密度是H2的43倍;将a g该烃完全燃烧,并使产生的产物全部依次通过下图装置,得到下表所列的实验结果(假设产生的气体产物完全被吸收).