题目内容
常用解热镇痛药-扑热息痛的结构简式为 HO-C6H4-NHCOCH3(C6H4表示苯环),对它的叙述有:①能与NaHCO3溶液反应;②能发生水解反应;③不能与浓溴水发生取代反应;④遇三氯化铁溶液显紫色.其中正确的是( )
| A、①和② | B、①和④ |
| C、②和③ | D、②和④ |
考点:有机物的结构和性质
专题:
分析:该有机物中含有酚羟基、肽键,所以具有酚、二肽的性质,能和NaOH溶液反应、能发生水解反应,能发生显色反应,据此分析解答.
解答:
解:该有机物中含有酚羟基、肽键,
①因为不含羧基,所以不能与NaHCO3溶液反应,故错误;
②含有肽键,所以能发生水解反应,故正确;
③因为含有酚羟基,所以能与浓溴水发生取代反应,故错误;
④因为含有酚羟基,所以遇三氯化铁溶液显紫色,故正确;
故选D.
①因为不含羧基,所以不能与NaHCO3溶液反应,故错误;
②含有肽键,所以能发生水解反应,故正确;
③因为含有酚羟基,所以能与浓溴水发生取代反应,故错误;
④因为含有酚羟基,所以遇三氯化铁溶液显紫色,故正确;
故选D.
点评:本题考查有机物官能团及其性质,明确官能团与性质关系即可解答,知道酚、肽的性质即可解答,题目难度不大.

练习册系列答案
相关题目
愈创木酚作原料合成香草醛的路线如图所示,下列说法正确 的是( )


| A、检验制得的香草醛中是否混有化合物3,可用氯化铁溶液 |
| B、化合物2在一定条件下可发生加聚反应 |
| C、理论上反应1→2中原子利用率100% |
| D、等物质的量的四种物质与足量NaOH溶液反应,消耗NaOH物质的量比为1:3:2:1 |
表明金属甲比金属乙活动性强的叙述正确的是( )
| A、在氧化还原反应中,甲失的电子比乙多 |
| B、将甲和乙用导线相连接,一同放入CuSO4溶液中,乙的表面有红色的铜析出 |
| C、同价态阳离子,甲比乙氧化性强 |
| D、将甲、乙组成原电池时,甲为正极 |
 前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )
前不久,各大媒体在显著的位置刊登了关于900t致癌大米的报道,主要是变质大米中存在的黄曲霉素使人体中的特殊基因发生突变,有转变成肝癌的可能性.它的结构如图所示,和l mol该化合物起反应的H2或NaOH的最大值分别是( )| A、5 mol,2 mol |
| B、7 mol,2 mol |
| C、6 mol,1 mol |
| D、7 mol,1 mol |
一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A、N2,H2和NH3的物质的量分数不再改变 |
| B、c(N2):c(H2):c(NH3)=1:3:2 |
| C、N2与H2的物质的量之和是NH3的物质的量2倍 |
| D、单位时间里每增加1molN2,同时增加3molH2 |
在一个恒容的密闭容器中进行如下反应:2SO2(g)+O2(g)?2SO3(g),已知反应过程中某一时刻SO2、SO3、O2的浓度分别为0.2mol/L、0.2mol/L、0.1mol/L,当该反应达到平衡时下列数据可能的是( )
| A、c(SO2)=0.4mol/L |
| B、c(SO2)=c(SO3)=0.15mol/L |
| C、c(SO2)=0.25mol/L |
| D、c(SO3)=0.4mol/L |
已知Co2O3在酸性溶液中易被还原成Co2+,且Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列叙述中,正确的是( )
| A、Cl2通入FeI2溶液中,可存在反应3Cl2+6FeI2=2FeCl3+4FeI3 |
| B、每1 mol Co2O3在酸性溶液中被氧化生成Co2+时转移2 mol e- |
| C、FeCl3溶液能使淀粉-KI试纸变蓝 |
| D、I2具有较强的氧化性,可以将Co2+氧化成Co2O3 |
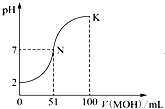 常温下向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02mol?L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题:
常温下向100mL 0.01mol?L-1 HA溶液中逐滴加入0.02mol?L-1 MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计).回答下列问题: