题目内容
尿素是含氮量最高的氮肥,工业上利用二氧化碳和氨气在一定条件下合成尿素.
(1)肥效相同时,尿素与硝酸铵的质量之比为 .尿素比其他氮肥的肥效期长,因为它在湿润的土壤里缓慢转化成易被作物吸收的碳酸铵,才起肥效,写出反应的化学方程式: .
(2)NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:

①第二步反应是 反应(填“放热”或“吸热”),理由是 .
②CO2(g)与NH3(g)合成尿素的热化学方程式为 .
(3)化工生产中,可以用尿素溶液吸收尾气中氯气,生成两种无污染气体,溶液pH明显降低.写出该反应的离子方程式: .
(4)已知:CH3CH2OH+CH3CH2OH
CH3CH2OCH2CH3+H2O,尿素在一定条件下也会失去氨而缩合,2分子尿素失去1分子氨形成二聚物,写出反应的化学方程式: .
(1)肥效相同时,尿素与硝酸铵的质量之比为
(2)NH3(g)与CO2(g)经过两步反应生成尿素,两步反应的能量变化示意图如下:

①第二步反应是
②CO2(g)与NH3(g)合成尿素的热化学方程式为
(3)化工生产中,可以用尿素溶液吸收尾气中氯气,生成两种无污染气体,溶液pH明显降低.写出该反应的离子方程式:
(4)已知:CH3CH2OH+CH3CH2OH
| H2SO4(浓) |
| 140℃ |
考点:反应热和焓变,化学方程式的书写
专题:化学反应中的能量变化
分析:(1)肥效相同,即含N元素质量相同;尿素与水反应生成碳酸铵,据原子守恒写出方程式;
(2)①从图象分析可知;
②由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的;
(3)氯气氧化了尿素生成二氧化碳、氮气和氯化氢;
(4)2分子尿素失氨气缩合,据原子守恒可以写出化学方程式.
(2)①从图象分析可知;
②由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的;
(3)氯气氧化了尿素生成二氧化碳、氮气和氯化氢;
(4)2分子尿素失氨气缩合,据原子守恒可以写出化学方程式.
解答:
解:(1)肥效相同,即含N元素质量相同,m(尿素)×
=m(硝酸铵)×
,即m(尿素)×
=m(硝酸铵)×
,所以,
=
,
尿素与水反应生成碳酸铵,据原子守恒写出方程式为:CO(NH2)2+2H2O═(NH4)2CO3,故答案为:
;CO(NH2)2+2H2O═(NH4)2CO3;
(2)①反应物的能量小于生成物,反应吸热,故答案为:吸热;反应物能量小于生成物;
②由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的,将两个反应相加可得2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol,
故答案为:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol;
(3)据题意可知,氯气氧化了尿素生成二氧化碳、氮气和氯化氢,反应的离子方程式为:CO(NH2)2+3Cl2+H2O═N2+CO2+6H++6Cl-,
故答案为:CO(NH2)2+3Cl2+H2O═N2+CO2+6H++6Cl-;
(4)2分子尿素失氨气缩合,结合乙醇脱水成醚,由原子守恒可知化学方程式为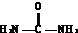 +
+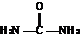

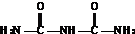 +NH3↑,故答案为:
+NH3↑,故答案为: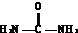 +
+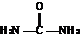

 +NH3↑.
+NH3↑.
| 2N |
| CO(NH2)2 |
| 2N |
| NH4NO3 |
| 28 |
| 60 |
| 28 |
| 80 |
| m(尿素) |
| m(硝酸铵) |
| 3 |
| 4 |
尿素与水反应生成碳酸铵,据原子守恒写出方程式为:CO(NH2)2+2H2O═(NH4)2CO3,故答案为:
| 3 |
| 4 |
(2)①反应物的能量小于生成物,反应吸热,故答案为:吸热;反应物能量小于生成物;
②由图示可知,两步反应的完成的热效应与一步完成的热效应是相同的,将两个反应相加可得2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol,
故答案为:2NH3(g)+CO2(g)═CO(NH2)2(s)+H2O(l)△H=-134 kJ/mol;
(3)据题意可知,氯气氧化了尿素生成二氧化碳、氮气和氯化氢,反应的离子方程式为:CO(NH2)2+3Cl2+H2O═N2+CO2+6H++6Cl-,
故答案为:CO(NH2)2+3Cl2+H2O═N2+CO2+6H++6Cl-;
(4)2分子尿素失氨气缩合,结合乙醇脱水成醚,由原子守恒可知化学方程式为
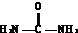 +
+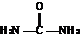

 +NH3↑,故答案为:
+NH3↑,故答案为: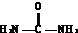 +
+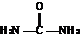

 +NH3↑.
+NH3↑.
点评:本题考查了据化学式的计算、化学方程式书写、据图象分析吸热反应、热化学方程式书写、离子方程式书写等等,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
将10mol A和5mol B放入10L真空箱内,某温度下发生反应:3A(气)+B(气)?2C(气)在最初0.2s内,消耗A的平均速率为0.06mol?(L?S)-1,则在0.2s时,真空箱中C的物质的量是( )
| A、0.04mol |
| B、0.08mol |
| C、0.12mol |
| D、0.8mol |
下列反应中,不属于氧化还原反应的是( )
| A、3Cl2+6KOH═5KCl+KClO3+3H2O |
| B、2FeBr2+3Cl2═2FeCl3+2Br2 |
| C、SnCl4+2H2O═SnO2+4HCl |
| D、Ca(OH )2+CO2═CaCO3↓+H2O |
元素M的最高正价和负价的绝对值之差为6,M、N的离子具有相同的电子排布,则M、N所形成的化合物可能是( )
| A、MgF2 |
| B、MgCl2 |
| C、CaCl2 |
| D、CaBr2 |
准确量取21.00mL KMnO4溶液,可选用的仪器是( )
| A、25mL量筒 |
| B、25mL酸式滴定管 |
| C、25mL碱式滴定管 |
| D、有刻度的50mL烧杯 |
下列物质中,不含有硅酸盐的是( )
| A、水玻璃 | B、硅芯片 |
| C、粘土 | D、平板玻璃 |
 碳酸镁晶须是一种新型的吸波隐形材料中的增强材料.已知某碳酸镁晶须样品的组成为MgCO3?nH2O (n为1~5的正整数),通过对其进行热重分析得到如图所示的热重曲线,试根据曲线计算n=
碳酸镁晶须是一种新型的吸波隐形材料中的增强材料.已知某碳酸镁晶须样品的组成为MgCO3?nH2O (n为1~5的正整数),通过对其进行热重分析得到如图所示的热重曲线,试根据曲线计算n=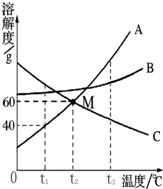 如图是常见固体物质的溶解度曲线,根据图示回答:
如图是常见固体物质的溶解度曲线,根据图示回答: