题目内容
19.已知:在273K,101Kpa的条件下,某气体:①质量为m,②相对分子质量为M,③体积为V,④密度为ρ,⑤所含分子数为N(阿伏伽德罗常数为NA),通过以上条件无法求出该气体物质的量的是( )| A. | ①② | B. | ③ | C. | ⑤ | D. | ②④ |
分析 根据气体的物质的量计算公式n=$\frac{m}{M}$=$\frac{V}{Vm}$来计算即可.
解答 解:根据气体的物质的量计算公式n=$\frac{m}{M}$=$\frac{V}{Vm}$=$\frac{N}{{N}_{A}}$,在273K,101Kpa的条件下Vm是一定值,所以根据①②可以计算气体的物质的量;根据③、⑤也可以分别代入公式计算计算,故选D.
点评 本题考查学生物种的量的计算方法,注意公式的灵活应用是关键,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.实验室进行中和热测定的实验时除需要大烧杯(500mL)、小烧杯(100mL)外,所用的其他仪器和试剂均正确的一组是( )
| A. | 0.50 mol•L-1 盐酸,0.50 mol•L-1 NaOH溶液,100 mL量筒1个 | |
| B. | 0.50 mol•L-1 盐酸,0.55 mol•L-1 NaOH溶液,100 mL量筒2个 | |
| C. | 0.50 mol•L-1 盐酸,0.55 mol•L-1 NaOH溶液,50 mL量筒1个 | |
| D. | 0.50 mol•L-1 盐酸,0.55 mol•L-1 NaOH溶液,50 mL量筒2个 |
11.下列溶液中离子一定能够大量共存的是( )
| A. | 使甲基橙变红的溶液中:NH4+、NO3-、Na+、SO42- | |
| B. | 无色透明的溶液中:Ba2+、H+、MnO4-、Br- | |
| C. | 能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- | |
| D. | 加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- |
9.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 标准状况下,22.4 L SO3中含有O数目为3.0NA | |
| B. | 常温常压下,12.2 gNaHSO4中含有离子总数为0.3NA | |
| C. | 在1 L 0.1 mol•L-1碳酸钠溶液中,阴离子总数大于0.1NA | |
| D. | 某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
 .
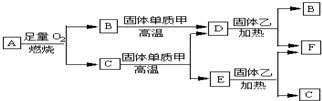
. 以下均为中学化学常见物质,存在如图转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.
以下均为中学化学常见物质,存在如图转化关系(部分产物已省略).通常C为气体单质,G为紫黑色固体单质.实验室中,常用固体E在B的催化下加热制取气体单质H.