题目内容
9.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )| A. | 标准状况下,22.4 L SO3中含有O数目为3.0NA | |
| B. | 常温常压下,12.2 gNaHSO4中含有离子总数为0.3NA | |
| C. | 在1 L 0.1 mol•L-1碳酸钠溶液中,阴离子总数大于0.1NA | |
| D. | 某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
分析 A、标况下,三氧化硫为固体;
B、求出NaHSO4的物质的量,然后根据1molNaHSO4中含1mol钠离子和1mol硫酸氢根离子来分析;
C、碳酸钠溶液中,碳酸根离子水解,导致溶液中阴离子数目增多;
D、合成氨的反应为可逆反应,不能进行彻底.
解答 解:A、标况下,三氧化硫为固体,不能根据其气体摩尔体积来计算其物质的量,故A错误;
B、12.2gNaHSO4的物质的量为0.1mol,而1molNaHSO4中含1mol钠离子和1mol硫酸氢根离子,故0.1mol硫酸氢钠中含0.2mol离子即0.2NA个,故B错误;
C、100mL 1mol•L-1 Na2CO3溶液中含有溶质碳酸钠0.1mol,由于碳酸根离子水解,溶液中阴离子数目大于0.1mol,阴离子总数大于0.1NA,故C正确;
D、合成氨的反应为可逆反应,不能进行彻底,故转移的电子数小于0.6NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.已知:在273K,101Kpa的条件下,某气体:①质量为m,②相对分子质量为M,③体积为V,④密度为ρ,⑤所含分子数为N(阿伏伽德罗常数为NA),通过以上条件无法求出该气体物质的量的是( )
| A. | ①② | B. | ③ | C. | ⑤ | D. | ②④ |
17.下列各组中的物质作用时,反应条件或反应物的量发生变化,对产物无影响的是( )
| A. | Na+O2 | B. | Cu+Cl2 | C. | NaOH溶液+CO2 | D. | C+O2 |
4.反应X(g)+Y(s)?2Z(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率和平衡都没有影响的是( )
| A. | 升高温度 | B. | 增加Y的用量 | C. | 减小压强 | D. | 使用催化剂 |
14.下列叙述正确的是( )
| A. | CO2的摩尔质量为44g | |
| B. | 1mol物质的质量等于该物质的相对分子质量或相对原子质量 | |
| C. | 在标准状况下,0.3molH2和0.7molN2 组成的混合气体的体积约为22.4L | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
1.下列仪器不能加热的是( )
| A. | 燃烧匙、蒸发皿 | B. | 圆底烧瓶、坩埚 | C. | 量筒、容量瓶 | D. | 试管、锥形瓶 |
19.下列叙述不正确的是( )
| A. | 生铁中含有碳,抗腐蚀能力比纯铁弱 | |
| B. | 在铁制品上镀铜时,石墨为阳极,铁制品作阴极,铜盐为电镀液 | |
| C. | 用锡焊接的铁质器件,焊接处易生锈 | |
| D. | 燃气灶上的炒锅支架容易生锈,主要是由于高温下铁易发生“化学腐蚀” |

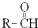 +
+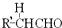 $\stackrel{OH-}{→}$
$\stackrel{OH-}{→}$ (-R、-R’表示氢原子或烃基)用B和C为原料按如下路线合成A:
(-R、-R’表示氢原子或烃基)用B和C为原料按如下路线合成A: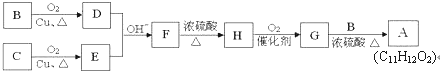
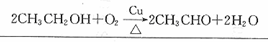
 .
.
 .
.