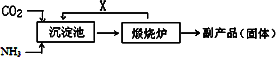
题目内容
将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:2H2(气)+CO(气)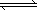 CH3OH(气),6秒时体系达到平衡,此时容器内气体的物质的量为开始时的0.6倍,求(1)H2的反应速率________;
CH3OH(气),6秒时体系达到平衡,此时容器内气体的物质的量为开始时的0.6倍,求(1)H2的反应速率________;
(2)CO的转化率________;
(3)求相同条件下CH3OH(气)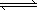 2H2(气)+CO(气)的平衡常数K________.
2H2(气)+CO(气)的平衡常数K________.
解析:
|
(1)v(H2)=1.2 mol·L-1·s-1(3分) (2)α(CO)=60%(3分) (3)K=15.36(4分) |

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案|
将8 mol H2和2 mol N2充入2 L密闭容器中,在一定条件下进行合成氨的反应,4 min后反应达到平衡,测得容器中还有5.6 mol H2.下列计算结果错误的是 | |
A. |
v(H2)=0.3 mol·L-1·min-1 |
B. |
H2的转化率为25% |
C. |
平衡时,NH3的物质的量浓度为0.8 mol/L |
D. |
反应前后的压强比为25∶21 |
| |||||||||||||||||||||||