题目内容
3.下列离子方程式的书写正确的是( )| A. | MgCl2溶液中加入足量的氨水:Mg2++2OH-═Mg (OH)2↓ | |
| B. | 向醋酸溶液中滴加NaOH溶液:OH-+H+═H2O | |
| C. | 金属钠加入水中:Na+2H2O═Na++2OH-+H2↑ | |
| D. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-═CO32-+H2O |
分析 A.一水合氨在离子反应中保留化学式;
B.醋酸在离子反应中保留化学式;
C.电子、电荷不守恒;
D.反应生成碳酸钠和水.
解答 解:A.MgCl2溶液中加入足量的氨水的离子反应为Mg2++2NH3.H2O═Mg (OH)2↓+2NH4+,故A错误;
B.向醋酸溶液中滴加NaOH溶液的离子反应为OH-+CH3COOH═CH3COO-+H2O,故B错误;
C.金属钠加入水中的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故C错误;
D.NaHCO3溶液与NaOH溶液反应的离子反应为OH-+HCO3-═CO32-+H2O,故D正确;
故选D.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
17.“绿色化学”要求在化工合成过程中,目标产物对反应物的原子利用率达到100%,下列反应类型最符合这一要求的是( )
| A. | 卤代反应 | B. | 加聚反应 | C. | 酯化反应 | D. | 消去反应 |
18.用下列实验装置进行相应实验,能达到实验目的是( )

| A. | 用图a所示装置用除去淀粉溶液中的NaCl | |
| B. | 用图b所示装置配制100mL0.100mol•L-1稀盐酸 | |
| C. | 图c所示装置可用于从碘水中分离出I2 | |
| D. | 图d所示装置可用于CaCO3和稀盐酸制取少量的CO2气体 |
18.下列说法正确的是( )
| A. | 硫完全燃烧生成二氧化硫时,放出的热量为硫的标准燃烧热 | |
| B. | 在101kPa时,1mol碳燃烧所放出的热量为碳的标准燃烧热 | |
| C. | 在101kPa时,由2CO(g)+O2(g)═2CO2(g)△H=-566 kJ•mol-1,可知CO的标准燃烧热为283 kJ•mol-1 | |
| D. | 乙炔的标准燃烧热为1299.6 kJ•mol-1,则2CH2(g)+5O2(g)═4CO2(g)+2H2O(g)反应的△H=-2 599.2 kJ•mol-1 |
8.分类法在化学学科发展中起到了非常重要的作用,下列分类标准合理的是( )
| A. | 根据是否含有氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据反应前后是否有元素化合价变化,可将化学反应分为氧化还原反应和非氧化还原反应 |
12.下列说法正确的是( )
| A. | 按系统命名法,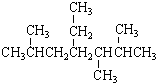 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,邻二甲苯、间二甲苯、对二甲苯的沸点依次增大 | |
| C. | 已知1mol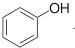 可以与1molNaOH发生反应.则1mol 可以与1molNaOH发生反应.则1mol 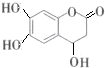 与足量的NaOH溶液发生反应时,需消耗4molNaOH 与足量的NaOH溶液发生反应时,需消耗4molNaOH | |
| D. | 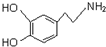 属于氨基酸,既能与强酸反应,又能与强碱反应 属于氨基酸,既能与强酸反应,又能与强碱反应 |