��Ŀ����
���á���ѧ����ת�Ʒ����Ʊ�TaS2���壬ij�¶��µ�2L�����ܱ������м���һ���� �� I2��g����TaS2��s���������·�Ӧ��TaS2��s��+2I2��g��?TaI4��g��+S2��g����H=a kJ?mol-1 ����ƽ��ʱ��TaS2��s����I2��g����TaI4��g����S2��g�������ʵ����ֱ�Ϊ3mol��2mol��2mol��2mol��
��1����Ӧ����ƽ�ⳣ������ʽK=
��2�������¶��¸�������ijʱ��TaS2��s����I2��g����TaI4��g����S2��g�������ʵ����ֱ�Ϊ2mol��2mol��4mol��4mol�����ʱ��ƽ���� �������Ӧ�����淴Ӧ�����ƶ���v�� v�棨���������=����������
��3���ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���±���
�÷�Ӧ�ġ�H 0�����������=����������
��4��40��ʱ����ú����ܱ������м���2mol I2��g����4mol TaS2��s����I2��g����ƽ��ת����Ϊ д��������̣��������С�����1λ��
��1����Ӧ����ƽ�ⳣ������ʽK=
��2�������¶��¸�������ijʱ��TaS2��s����I2��g����TaI4��g����S2��g�������ʵ����ֱ�Ϊ2mol��2mol��4mol��4mol�����ʱ��ƽ����
��3���ڲ�ͬ�¶��£��÷�Ӧ��ƽ�ⳣ��K���±���
| �¶�/�� | 40 | 80 | 200 |
| ƽ�ⳣ��K | 1 | 1.5 | 4 |
��4��40��ʱ����ú����ܱ������м���2mol I2��g����4mol TaS2��s����I2��g����ƽ��ת����Ϊ
���㣺��ѧƽ�ⳣ���ĺ���,��ѧƽ���Ӱ������,��ѧƽ��ļ���
ר�⣺��ѧƽ��ר��
��������1��ƽ��ʱ����Ũ�ȵ���֮�����Ϸ�Ӧ��Ũ����֮����
��2��Ũ������ƽ��Ĵ�С��Ƚϣ��õ���Ӧ���ƶ�����
��3���¶ȸı�ƽ�ⳣ���ı仯��
��4��Ӧ������ʽ����I2��g����ƽ��ת���ʣ�
��2��Ũ������ƽ��Ĵ�С��Ƚϣ��õ���Ӧ���ƶ�����
��3���¶ȸı�ƽ�ⳣ���ı仯��
��4��Ӧ������ʽ����I2��g����ƽ��ת���ʣ�
���
�⣺��1��ƽ��ʱ����Ũ�ȵ���֮�����Ϸ�Ӧ��Ũ����֮����K=
���ʴ�Ϊ��K=
��
��2��K=
=1����Q=
=4��Q��K����Ӧ���淴Ӧ�����ƶ���v����v�棬�ʴ�Ϊ���淴Ӧ������
��3���ɱ���֪���¶�����K�������Ӧ�����ȷ�Ӧ���ʴ�Ϊ������
��4��TaS2��s��+2I2��g��?TaI4��g��+S2��g��
��ʼŨ�ȣ�mol/L����1 0 0
ת��Ũ�ȣ�mol/L����2x x x
ƽ��Ũ�ȣ�mol/L����1-2x x x
����K=
=1�����x=
����I2��g����ƽ��ת����Ϊ��
��100%=66.7%��
| c(TaI4)c(S2) |
| c2(I2) |
| c(TaI4)c(S2) |
| c2(I2) |
��2��K=
| ||||
(
|
| ||||
(
|
��3���ɱ���֪���¶�����K�������Ӧ�����ȷ�Ӧ���ʴ�Ϊ������
��4��TaS2��s��+2I2��g��?TaI4��g��+S2��g��
��ʼŨ�ȣ�mol/L����1 0 0
ת��Ũ�ȣ�mol/L����2x x x
ƽ��Ũ�ȣ�mol/L����1-2x x x
����K=
| x��x |
| (1-2x)2 |
| 1 |
| 3 |
2��
| ||
| 1 |
���������⿼�黯ѧƽ�ⳣ������ʽ���ж�ƽ����ƶ�����Ӧ����ЧӦ���Լ�����ƽ�ⳣ����ת���ʣ��Ƚ����ף�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
�����£���������Һ�з������·�Ӧ
��2FeCl3+2KI=2FeCl2+2KCl+I2
��2FeCl2+Cl2=2FeCl3
��2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O��
�ɴ��ж�����˵����ȷ���ǣ�������
��2FeCl3+2KI=2FeCl2+2KCl+I2
��2FeCl2+Cl2=2FeCl3
��2KMnO4+16HCl=2KCl+2MnCl2+5Cl2��+8H2O��
�ɴ��ж�����˵����ȷ���ǣ�������
| A����������ǿ����˳���ǣ�KMnO4��Cl2��Fe3+��I2 |
| B����ԭ����ǿ����˳���ǣ�Mn2+��Cl-��Fe2+��I- |
| C��I--��Fe3+������Һ�з���������ԭ��Ӧ |
| D������Һ�п��Է���2KCl+I2=Cl2+2KI��Ӧ |
�����й�ʵ���˵������ȷ���ǣ�������
| A�������������У��¶ȼƵ�ˮ����λ��������ƿ֧�ܿڴ���Ϊ�˲����ֵķе� |
| B�����ؽᾧ������������У������ǣ������ܽ⣬���ȹ��ˣ���ȴ�ᾧ |
| C���������Ҵ�����ȡ������ȡ��ˮ�е��嵥�� |
| D�������ܽ�ˮ�����£���ˮ������ |
�ĸ���ͬ�����ڲ�ͬ�����½��кϳɰ���Ӧ��������������ͬʱ���ڲⶨ�Ľ���жϣ����ɰ������������ǣ�������
| A����H2��ʾ�ķ�Ӧ����Ϊ0.1mol?L-1?min-1 |
| B����N2��ʾ�ķ�Ӧ����Ϊ0.04mol?L-1?s-1 |
| C����N2��ʾ�ķ�Ӧ����Ϊ0.2mol?L-1?s-1 |
| D����NH3��ʾ�ķ�Ӧ����Ϊ0.3mol?L-1?s- |
����ˮ�д��ڶ��ַ��Ӻ����ӣ������ڲ�ͬ�ķ�Ӧ�б��ָ��Ե����ʣ�����ʵ������ͽ���һ������ȷ���ǣ�������
| A������ˮ�м�����ɫ����һ�����ɫ������ɫ��˵����Һ����Cl2���� |
| B��������ˮ������ɫʯ����ֽ�ϣ���ֽ�ȱ��ɫ����ɫ��˵�� Cl2��Ư���� |
| C������۵⻯����Һ�м�����ˮ����Һ��Ϊ��ɫ����֤��Cl2��������ǿ��I2 |
| D������NaOH��Һ����ˮ����ɫ��ʧ��˵����HClO���Ӵ��� |
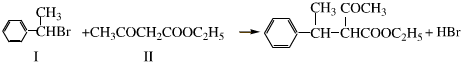
 ��һ����
��һ���� �ܷ������Ƣٵķ�Ӧ�������л��������������Ľṹ��ʽΪ
�ܷ������Ƣٵķ�Ӧ�������л��������������Ľṹ��ʽΪ ijУ��ѧ��ȤС���ڼ�������������Ũ������������̷�Ӧ����ȡ���ռ�����ʵ��װ����ͼ
ijУ��ѧ��ȤС���ڼ�������������Ũ������������̷�Ӧ����ȡ���ռ�����ʵ��װ����ͼ