题目内容
(1)在25℃、101 kPa下,1 g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:________.
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1=-702 kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2=-182 kJ/mol
由此可知ZnO(s)+Hg(l)=Zn(s)+HgO(s) ΔH3=________.
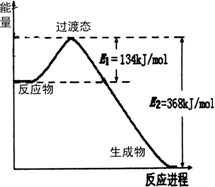
(3)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态.下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:________.
答案:
解析:
解析:
|
(1)CH4(g)+2O2(g) (2)ΔH3=+260 kJ/mol (3)NO2(g)+CO(g) |

练习册系列答案
相关题目