题目内容
已知一种混合气体由H2、N2两种气体按照体积比3:1组成,该混合气体的平均相对分子质量为( )
| A、30 | B、15 | C、34 | D、8.5 |
考点:物质的量的相关计算,相对分子质量及其计算
专题:
分析:混合气体由H2、N2两种气体按照体积比3:1组成,设物质的量分别为3mol、1mol,结合
=
计算.
. |
| M |
| m总 |
| n总 |
解答:
解:混合气体由H2、N2两种气体按照体积比3:1组成,设物质的量分别为3mol、1mol,
则混合气体的平均摩尔质量为
=8.5g/mol,
摩尔质量与相对分子质量的数值相等,则该混合气体的平均相对分子质量为8.5,
故选D.
则混合气体的平均摩尔质量为
| 2g/mol×3mol+28g/mol×1mol |
| 3mol+1mol |
摩尔质量与相对分子质量的数值相等,则该混合气体的平均相对分子质量为8.5,
故选D.
点评:本题考查物质的量的计算,为高频考点,把握平均摩尔质量的计算公式及与相对分子质量的关系为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
镁粉在焰火、闪光粉中是不可少的原料,工业制造镁粉的最后一步是将镁蒸气在气体中冷却,下列可作为冷却气体的是( )
| A、空气 |
| B、O2 |
| C、CO2 |
| D、H2 |
下列各组离子在水溶液中能大量共存的是( )
| A、Cu2+、Ba2+、Cl-、SO42- |
| B、H+、CO32-、NO3-、K+ |
| C、Mg2+、Ag+、NO3-、Cl- |
| D、OH-、Cl-、Na+、CO32- |
如图BF3与一定量的水形成(H2O)2?BF3晶体Q,Q在一定条件下可转化为R,反应过程中新形成的化学键包括( )


| A、离子键 | B、配位键 |
| C、金属键 | D、氢键 |
下列各组物质发生变化时,所克服的粒子间作用力属于同种类型的是( )
| A、氯化铵晶体和二氧化硅的熔化 |
| B、碘和干冰的升华 |
| C、氯化钾和氯化氢溶解于水 |
| D、溴和汞的气化 |
把质量分数为14%的KOH溶液蒸发掉100克水后变为80毫升质量分数为28%的KOH溶液,则蒸发后溶液的物质的量浓度为( )
| A、6.00mol/L |
| B、6.25mol/L |
| C、3.50mol/L |
| D、7.00mol/L |
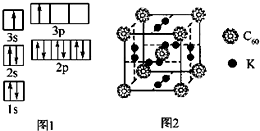 能源的发展日益成为全世界、全人类共同关心的问题.
能源的发展日益成为全世界、全人类共同关心的问题.