题目内容
|
将0.5 mol CO2通入200 g 10%的NaOH溶液中,充分反应后,生成的盐为 | |
| [ ] | |
A. |
只有 Na2CO3 |
B. |
只有 NaHCO3 |
C. |
既有 Na2CO3,又有NaHCO3 |
D. |
无法确定 |

|
下列热化学方程式或离子方程式中,正确的是 | |
| [ ] | |
A. |
甲烷的标准燃烧热为-890.3 kJ/mol,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1 |
B. |
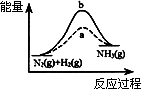
500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) |
C. |
HCl和NaOH反应中和热ΔH=-57.3 kJ·mol-1, 则H2SO4和Ca(OH)2反应热ΔH=2×(-57.3)kJ·mol-1 |
D. |
氧化铝溶于NaOH溶液:Al2O3+2OH- |
|
下列说法正确的是 | |
| [ ] | |
A. |
甲烷的标准燃烧热为-890.3 KJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g) |
B. |
500℃,30 Mpa下,将0.5 mol N2和1.5 H2置于密闭的容器中充分反应生成NH3(g),放热19.3 KJ,其热化学方程式为: N2(g)+3H2(g) |
C. |
常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
D. |
同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH不同 |
|
下列说法正确的是 ①活性炭、SO2和HClO都具有漂白作用,且漂白的化学原理相同 ②第ⅠA族元素铯的两种同位素137Cs比133Cs多4个质子 ③因为氧化性:HClO>稀H2SO4,所以非金属性:Cl>S ④泥水、淀粉溶液、盐酸分别属于悬浊液、胶体、溶液 ⑤碳酸氢根离子的电离方程式:HCO ⑥从上到下,卤族元素的非金属性逐渐减弱,故氢卤酸的酸性依次减弱 ⑦500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3H2(g) | |
| [ ] | |
A. |
全部 |
B. |
④⑤ |
C. |
②③④⑦ |
D. |
②④⑦ |
 2NH3(g);ΔH=-38.6 kJ·mol-1
2NH3(g);ΔH=-38.6 kJ·mol-1 2NH3(g) ΔH=-38.6 KJ·mol-1
2NH3(g) ΔH=-38.6 KJ·mol-1