题目内容
如图所示的实验操作和方法不是用来分离物质的是( )
A、 |
B、 |
C、 |
D、 |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:化学实验基本操作
分析:常用的混合物分离方法为:过滤、蒸发、萃取、分液、蒸馏、渗析等,而选项D为气密性检查,以此来解答.
解答:
解:A.图为蒸发实验,用于可溶性固体与液体的分离,故A不选;
B.图为分液实验,用于分层的混合物的分离,故B不选;
C.图为过滤实验,用于不溶性固体与液体的分离,故C不选;
D.图为气密性检查实验操作,不能用于混合物分离,故D选;
故选D.
B.图为分液实验,用于分层的混合物的分离,故B不选;
C.图为过滤实验,用于不溶性固体与液体的分离,故C不选;
D.图为气密性检查实验操作,不能用于混合物分离,故D选;
故选D.
点评:本题考查混合物分离提纯的方法及选择,为高频考点,把握实验装置及实验原理为解答的关键,侧重分离方法及原理的考查,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
下列粒子浓度关系不正确的是( )
| A、Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| B、NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| C、pH=2的盐酸与pH=12的氨水以任意比例混合所得溶液中:c(H+)+c(NH4+)=c(OH-)+c(Cl-) |
| D、等物质的量浓度的CH3COOH和CH3COONa溶液等体积混合后所得溶液中:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) |
下列各组离子一定能大量共存的是( )
| A、在c(HCO3-)=0.1mol?L-1的溶液中:NH4+、Al3+、Cl-、NO3- |
| B、在与铝反应放出氢气的溶液中:K+、SO42-、Br-、Na+ |
| C、25℃,在由水电离出的c(H+)=10-13mol?L-1的溶液中:NH4+、Al3+、SO42-、NO3- |
| D、在能使甲基橙变红的溶液中:K+、Fe2+、Cl-、NO3- |
下列说法正确的是( )
| A、PM2.5微粒虽然比胶体粒子小,但由于表面积大,能吸附大量的有毒、有害物质,入肺后对人体会产生很大的危害 |
| B、苯丙氨酸可以与NaOH溶液或HCl溶液反应形成内盐,内盐的形成是由氢键所致 |
| C、石油催化裂化的主要目的是提高汽油等轻质油的产量与质量;石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
| D、李比希法、钠融法、铜丝燃烧法、元素分析仪均可帮助人们确定有机化合物的元素组成和空间结构 |
化学方程式可简明地体现元素及其化合物的性质.已知:
氧化还原反应:
2FeCl3+2HI═2FeCl2+I2+2HCl;2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O;2FeCl2+Cl2═2FeCl3
复分解反应:
2CH3COOH+K2CO3═2CH3COOK+CO2↑+H2O;KCN+CO2+H2O═HCN+KHCO3
热分解反应:
4NaClO
3NaCl+NaClO4;NaClO4
NaCl+2O2↑
下列说法不正确是( )
氧化还原反应:
2FeCl3+2HI═2FeCl2+I2+2HCl;2Co(OH)3+6HCl═2CoCl2+Cl2↑+6H2O;2FeCl2+Cl2═2FeCl3
复分解反应:
2CH3COOH+K2CO3═2CH3COOK+CO2↑+H2O;KCN+CO2+H2O═HCN+KHCO3
热分解反应:
4NaClO
| ||
| ||
下列说法不正确是( )
| A、氧化性(酸性溶液):Co(OH)3>FeCl3>I2 |
| B、还原性(酸性溶液):FeCl2>HI>HCl |
| C、酸性(水溶液):CH3COOH>H2CO3>HCN |
| D、热稳定性:NaCl>NaClO4>NaClO |
下列化学反应的离子方程式,书写正确的是( )
| A、碳酸钙与稀盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氢氧化铁溶于盐酸:Fe(OH)3+3H+═Fe3++3H2O |
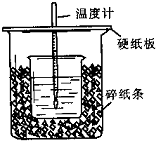 某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )
某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中反应,通过测定该过程中所放出的热量计算中和热.下列说法中正确的是( )| A、图中实验装置缺少环形玻璃搅拌棒 |
| B、烧杯间填满碎纸条的作用是固定小烧杯 |
| C、大小烧杯的杯口不相平,对实验结果无影响 |
| D、大烧杯上不盖硬纸板,求得的中和热△H会偏小 |
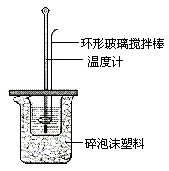 已知测定中和热的实验步骤如下:①量取30mL 0.5mol/L硫酸倒入小烧杯中,测量温度; ②量取50mL 0.5mol/L NaOH溶液,测量温度; ③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.回答下列问题
已知测定中和热的实验步骤如下:①量取30mL 0.5mol/L硫酸倒入小烧杯中,测量温度; ②量取50mL 0.5mol/L NaOH溶液,测量温度; ③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度.回答下列问题