题目内容
下列化学反应的离子方程式,书写正确的是( )
| A、碳酸钙与稀盐酸反应:CO32-+2H+═H2O+CO2↑ |
| B、铁跟稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
| C、铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ |
| D、氢氧化铁溶于盐酸:Fe(OH)3+3H+═Fe3++3H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.碳酸钙为难溶物,离子方程式中不能拆开,应该保留化学式;
B.铁与盐酸反应生成的是亚铁离子,不是铁离子;
C.根据质量守恒定律判断,离子方程式两边氧原子不守恒;
D.氢氧化铁为难溶物,离子方程式中需要保留化学式.
B.铁与盐酸反应生成的是亚铁离子,不是铁离子;
C.根据质量守恒定律判断,离子方程式两边氧原子不守恒;
D.氢氧化铁为难溶物,离子方程式中需要保留化学式.
解答:
解:A.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2H+=Ca2++H2O+CO2↑,故A错误;
B.Fe跟稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.Al粉投入到NaOH溶液中,反应生成偏铝酸钠和氢气,离子方程式必须满足质量守恒,正确的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑,故C错误;
D.氢氧化铁溶于盐酸生成氯化铁和水,反应的离子方程式为:Fe(OH)3+3H+═Fe3++3H2O,故D正确;
故选D.
B.Fe跟稀硫酸反应生成硫酸亚铁和氢气,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故B错误;
C.Al粉投入到NaOH溶液中,反应生成偏铝酸钠和氢气,离子方程式必须满足质量守恒,正确的离子方程式:2Al+2H2O+2OH-═2AlO2-+3H2↑,故C错误;
D.氢氧化铁溶于盐酸生成氯化铁和水,反应的离子方程式为:Fe(OH)3+3H+═Fe3++3H2O,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,该题为高考中的高频题,难度中等,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等;选项C为易错点,根据质量守恒定律或电子守恒进行判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
如图所示的实验操作和方法不是用来分离物质的是( )
A、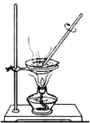 |
B、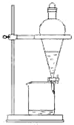 |
C、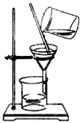 |
D、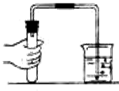 |
某烯烃跟氢气起加成反应的产物是2,2,3,4-四甲基戊烷,这样的单烯烃可能有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
下列化学用语表示正确的是( )
| A、HClO、KOH的结构式都可用X-Y-Z表示 |
B、O2-、Mg2+的结构中能量最高电子层的轨道表示式都可以用图表示: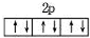 |
C、甲烷、四氯化碳的分子构型相似,均可以表示为: |
| D、分子式中n(C):n(H)=n:(2n+2)的物质不一定是烷烃 |
下列有关化学用语的使用正确的是( )
| A、Cl2通入石灰乳中制漂白粉的离子方程式:Cl2+2OH-═Cl-+ClO-+H2O | ||
| B、利用泡沫灭火器灭火时发生的反应:2Al3++CO32-+3H2O═2Al(OH)3↓+CO2↑ | ||
| C、已知离子的还原性:Sn2+>Fe2+,则可推测在溶液中能发生如下反应:Sn4++2Fe2+═2Fe3++Sn2+ | ||
D、298 K时,已知12g石墨完全燃烧生成CO2(g)放出393.5kJ热量,1mol CO完全燃烧放出283.5kJ热量,则一定有:C(s,石墨)+
|
下列说法正确的是( )
| A、丙炔分子中三个碳原子位于同一直线上 |
| B、丙烯与HCl加成只生成一种产物 |
| C、1mol丙烷在光照情况下,最多消耗4mol氯气 |
| D、丙烷中混有丙烯可用H2加热方法除去 |
合成氨反应中,若进口时N2、H2、NH3的体积之比为5:15:3,出口时N2、H2、NH3的体积之比为9:27:8,则N2的转化率为( )
| A、10% | B、20% |
| C、30% | D、40% |
如图甲池和乙池中的四个电极都是惰性材料,请根据图示判断下列说法正确的是( )
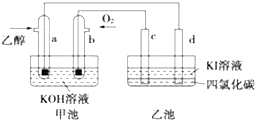

| A、两个装置之间没有盐桥,故不能形成电流 |
| B、a电极的电极反应式:C2H5OH+16OH--12e-═2CO32-+11H2O |
| C、一段时间后,乙池d电极周围的溶液呈现棕褐色 |
| D、乙池在反应前后溶液的pH不变 |
 为探究乙炔与溴的加成反应,
为探究乙炔与溴的加成反应,