题目内容
在一定体积的密闭容器中,进行如下化学反应:A(g)+3B(g)?2C(g)+D(s)△H,其化学平衡常数K与温度t的关系如下表:
请完成下列问题:
该反应的化学平衡常数表达式为K= .
判断该反应的△H 0(填“>”或“<”)
在一定条件下,不能判断该反应已达化学平衡状态的是 (填序号).
A.3v(B)(正)=2v(C)(逆)B.D的物质的量不变C.容器内压强保持不变D.混合气体的密度保持不变.
| t/K | 298 | 398 | 498 | … |
| K/(mol?L-1)-2 | 4.1×106 | 8.2×107 | K1 | … |
该反应的化学平衡常数表达式为K=
判断该反应的△H
在一定条件下,不能判断该反应已达化学平衡状态的是
A.3v(B)(正)=2v(C)(逆)B.D的物质的量不变C.容器内压强保持不变D.混合气体的密度保持不变.
考点:化学平衡状态的判断,化学平衡建立的过程
专题:化学平衡专题
分析:根据化学平衡常数的概念以及温度对化学平衡、化学平衡常数的影响判断;平衡状态的判断依据是正逆反应速率相等和各组分浓度保持不变的状态,据此判断.
解答:
解:因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=
;化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热;
A、反应速率之比等于其化学计量数之比,当2v(B)(正)=3v(C)(逆)时,反应达到平衡状态,故A错误;
B、D物质的量不变,说明各组分浓度不变,反应达到平衡状态,故B正确;
C、反应前后气体物质的量不同,容器内压强不变说明反应达到平衡状态,故C正确;
D、D为固态,反应正向进行时,气体质量减小,反应逆向进行,气体质量增大,所以气体密度不变说明反应达到平衡状态,故D正确;
故选A;
故答案为:
;>;A.
| [C]2 |
| [A]?[B]3 |
A、反应速率之比等于其化学计量数之比,当2v(B)(正)=3v(C)(逆)时,反应达到平衡状态,故A错误;
B、D物质的量不变,说明各组分浓度不变,反应达到平衡状态,故B正确;
C、反应前后气体物质的量不同,容器内压强不变说明反应达到平衡状态,故C正确;
D、D为固态,反应正向进行时,气体质量减小,反应逆向进行,气体质量增大,所以气体密度不变说明反应达到平衡状态,故D正确;
故选A;
故答案为:
| [C]2 |
| [A]?[B]3 |
点评:本题考查了化学平衡常数的表达式以及影响其大小的因素、化学平衡状态的判断,题目难度不大.

练习册系列答案
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案
相关题目
只用一种试剂一次鉴别乙醇、乙酸、苯、葡萄糖溶液,最好选用( )
| A、银氨溶液 | B、新制氢氧化铜悬浊液 |
| C、浓溴水 | D、金属钠 |
维生素C的结构如图所示:则在维生素C中所含的官能团种类有( )


| A、三种 | B、四种 | C、五种 | D、六种 |
下列反应,其产物的颜色按红、红褐、淡黄、蓝色顺序排列的是( )
①金属钠在纯氧中燃烧
②Fe2(SO4)3溶液中滴入NaOH溶液
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用洒精中.
①金属钠在纯氧中燃烧
②Fe2(SO4)3溶液中滴入NaOH溶液
③FeCl3溶液中滴入KSCN溶液
④无水硫酸铜放入医用洒精中.
| A、②③①④ | B、③②①④ |
| C、③①②④ | D、①②③④ |
由苯乙烯和羟基乙酸乙酯(HO-CH2-COOCH2CH3)组成的混合物中,若碳元素的质量分数为70%,那么氢元素的质量分数约为( )
| A、4.6% | B、7.7% |
| C、15.6% | D、无法计算 |
对室温下体积相同,浓度均为0.1mol?L-1的盐酸和醋酸两种溶液分别采取下列措施.有关叙述中一定正确的是( )
| A、加入稀释100倍后,两溶液的pH相同 |
| B、加入NaOH固体恰好中和后,两溶液的pH相同 |
| C、加入足量的小苏打固体充分反应后,两溶液中产生的CO2一样多 |
| D、分别加入足量的锌粉充分反应,反应开始时两酸产生H2的反应速率相等 |


 aA、bB、cC、dD四种短周期元素,它们的原子序数有如下关系:c-b=b-a=1 且 b+c=d,B的最高价氧化物对应水化物为强酸.
aA、bB、cC、dD四种短周期元素,它们的原子序数有如下关系:c-b=b-a=1 且 b+c=d,B的最高价氧化物对应水化物为强酸.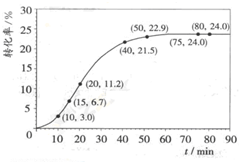 甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0
甲酸甲酯水解反应方程式为:HCOOCH3(l)+H2O(l)?HCOOH(l)+CH3OH(l);△H>0