题目内容
18.某实验小组欲制取氯酸钾,并测定其纯度.制取装置如图甲所示.请回答: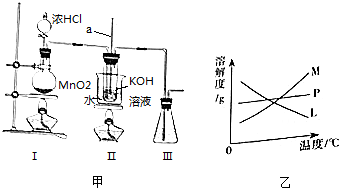
(1)Ⅱ中玻璃管a的作用为平衡压强.
(2)为了提高KOH的利用率,可将上述实验装置进行适当改进,其方法是在Ⅰ与Ⅱ之间连接盛有饱和食盐水的净化装置.
(3)反应完毕经冷却后,Ⅱ的大试管中有大量KClO3晶体析出.图乙中符合该晶体溶解度曲线的是M(填编号字母);要从Ⅱ的大试管中分离已析出晶体,下列仪器中不需要的是BDF(填仪器编号字母).
A.铁架台 B.长颈漏斗 C.烧杯 D.蒸发皿 E.玻璃棒 F.酒精灯
(4)上述制得的晶体中含少量KClO、KCl杂质.
已知:碱性条件下,ClO-有强氧化性,ClO3-很稳定;酸性条件下,ClO-、ClO3-都具有较强的氧化性.
为测定KClO3的纯度,进行如下实验:
步骤1:去上述晶体3.00g,溶于水配成100mL溶液.
步骤2:取20.00mL溶液于锥形瓶中,调至pH=10,滴加双氧水至不再产生气泡,煮沸.
步骤3:冷却后,加入足量KI溶液,再逐渐滴加入足量稀硫酸.
发生反应:ClO3-+I-+H+→Cl++I2+H2O(未配平)
步骤4:加入指示剂,用0.5000mol•L-1Na2S2O3标准溶液滴定至终点,消耗标准溶液48.00mL,发生反应:2S2O32-+I2═S4O62-+2I-.
①步骤2中用双氧水除去溶液中残留ClO-的离子方程式为ClO-+H2O2═H2O+Cl-+O2↑.
②该晶体中KClO3的质量分数为81.7%.
③若步骤2中未进行煮沸,则所测KClO3的质量分数偏高(填“偏低”、“偏高”或“无影响”)
分析 (1)Ⅱ中玻璃管a的作用是平衡压强,防止压强改变液体倒吸;
(2)装置Ⅰ是制备氯气的装置,生成的氯气中含有氯化氢和水蒸气,仪器进入装置Ⅱ,氯化氢也消耗氢氧化钾,需要通入前除去;
(3)在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,溶质的溶解度随温度的降低而降低,不溶性固体与液体的分离常采用过滤的方法;
(4)①用双氧水除去溶液中残留ClO-的反应是利用次氯酸根离子的强氧化性氧化过氧化氢生成氧气,本身被还原生成氯离子,结合原子守恒和电子守恒、电荷守恒配平书写;
②依据过程中的反应ClO3-+6I-+6H+=Cl-+3I2+3H2O和2S2O32-+I2═S4O62-+2I-,得到关系ClO3-~3I2~6S2O32-,结合实验过程中的数据计算;
③滴加双氧水至不再产生气泡,煮沸除去混有的氧气,避免氧气氧化碘离子为碘单质,消耗Na2S2O3标准溶液体积增大.
解答 解:(1))Ⅱ中玻璃管a的作用为平衡压强,防止压强改变液体倒吸,故答案为:平衡压强;
(2)装置Ⅰ是制备氯气的装置,生成的氯气中含有氯化氢和水蒸气,仪器进入装置Ⅱ,氯化氢也消耗氢氧化钾,为了提高KOH的利用率需要通入前除去,在Ⅰ与Ⅱ之间连接盛有饱和食盐水的净化装置,除去氯化氢气体,
故答案为:在Ⅰ与Ⅱ之间连接盛有饱和食盐水的净化装置;
(3)根据题中信息可知,在加热条件下,氯气与浓KOH溶液反应生成氯酸钾,在常温以下,氯气与稀NaOH溶液反应生成次氯酸钠,二者反应的浓度和温度都不相同,反应完毕经冷却后,②的试管中有大量晶体析出,说明溶质的溶解度随温度的降低而降低,只有M符合,不溶性固体与液体的分离常采用过滤的方法,过滤需要的仪器为烧杯、铁架台、玻璃棒、漏斗等,不需要的仪器为B.长颈漏斗、D.蒸发皿、F.酒精灯,
故答案为:M;BDF;
(4)①用双氧水除去溶液中残留ClO-的反应是利用次氯酸根离子的强氧化性氧化过氧化氢生成氧气,本身被还原生成氯离子,反应的离子方程式为:ClO-+H2O2═H2O+Cl-+O2↑,
故答案为:ClO-+H2O2═H2O+Cl-+O2↑;
②反应ClO3-+6I-+6H+=Cl-+3I2+3H2O和2S2O32-+I2═S4O62-+2I-,得到关系ClO3-~3I2~6S2O32-,注意溶液体积的关系,
ClO3-~3I2~6S2O32-,
1 6
n 0.500mol/L×0.0480L×$\frac{100}{20}$
n=0.02mol
晶体中KClO3的质量分数=$\frac{0.02mol×122.5g/mol}{3.00g}$×100=81.7%,
故答案为:81.7%;
③滴加双氧水至不再产生气泡,煮沸除去混有的氧气,避免氧气氧化碘离子为碘单质,消耗Na2S2O3标准溶液体积增大,所测KClO3的质量分数偏高,
故答案为:偏高.
点评 本题考查了物质组成、物质检验、物质分离的方法、实验基本操作和反应定量的计算等知识,题目难度中等.

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案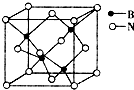 已知火箭所用燃料为肼(N2H4),氧化剂为过氧化氢,火箭部分构件采用钛合金材料.请回答下列问题:
已知火箭所用燃料为肼(N2H4),氧化剂为过氧化氢,火箭部分构件采用钛合金材料.请回答下列问题:(1)N2H4、H2O2的组成元素中第一电离能最大的元素是N.
(2)钛的原子序数是22,其基态原子的核外电子排布式为[Ar]3d24s2.
(3)1molN2H4分子中所含极性键的数目为4NA.
(4)H2O2受热易分解为H2O,H2O的空间构型为V形.其中心原子的杂化轨道类型为sp3.
(5)H2S和H2O2的主要物理性质如表所示:
| 物质 | 熔点/K | 沸点/K | 水中溶解度(标准状况) |
| H2S | 187 | 202 | 每升水中溶解2.6L |
| H2O2 | 272 | 423 | 以任意比互溶 |
(6)氧化镁和氮化硼均可用作返回舱的热屏蔽材料,晶格能:氧化镁大于氧化钙(填“大于”或“小于”).
(7)立方氮化硼的晶胞如图所示,则处于晶胞顶点的原子的配位数为4,若晶胞边长为a pm,则立方氮化硼晶胞的密度是$\frac{100}{{{N_A}{{(a×{{10}^{-10}})}^3}}}$g•cm-3(只要求列算式,阿伏伽德罗常数为NA).
| A. | 常温下,1 L 0.1 mol•L-1 的NH4NO3溶液中氮原子数为0.2NA | |
| B. | 标准状况下,2.24 L己烷中共价键数目为1.9NA | |
| C. | 室温下,28.0 g乙烯和丁烯的混合气体中含有的碳原子数为2NA | |
| D. | 足量Fe与标准状况下22.4 L Cl2充分反应,转移的电子数为2NA |
| A. | +45 kJ/mol | B. | +32.7 kJ/mol | C. | -45 kJ/mol | D. | 无法计算 |
(1)某恒容密闭容器中存在如下反应:C(s)+2NO(g)?N2(g)+CO2(g)△H.维持温度不变,测得不同时刻几种气体物质的浓度如下表所示:
| 时间(min) 浓度(mol•L-1) | 0 | 5 | 10 | 15 | 25 | 30 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | a | a | b | b |
| CO2 | 0 | 0.21 | a | a | 0.36 | 0.36 |
②表中25min的数据变化与反应进行到22min时改变了反应体系中的某一条件有关,则b=0.36,改变的条件可能是c.
a.加入一定量的活性炭
b.通入一定量的N2
c.适当缩小容器的体积
③若15min时升高温度,达到平衡时容器中NO、N2、CO2的浓度之比为5:3:3,则△H<0(填“>”、“=”或“<”).
(2)NH3催化还原氮氧化物(产物是N2、H2O)是目前广泛采用的烟气脱氮技术
①当废气中NO2、NO的体积分数相等时脱氮率最高,若此情况下生成1molN2时反应放出的热量为akJ,则对应的热化学方程式为2NH3(g)+NO(g)+NO2(g)=2N2(g)+3H2O(g)△H=-2akJ/mol.
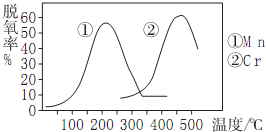
②如图使用不同催化剂时的脱氮率,则脱氮时最佳的温度、催化剂应是Mn、200℃左右.
(3)用石灰浆作吸收剂也可脱去废气中的SO2,若处理结束时,测得吸收液中c(Ca2+)=0.70mol/L,则c(SO32-)=2.0×10-7 mol/L (已知Ksp(CaSO3)=1.4×10-7).
| A. | BeCl2 | B. | C2H2 | C. | CO2 | D. | NH3 |